1�������� ��ԭ�������ֻ��һ�����ӣ��ڷ�Ӧ��ʧȥ���������γ�+1�۵�Na+��Ϊ����֤����ˮ��Ӧ�õ�����Na+������Na2+��ijѧϰС���������������ʵ�鷽��������֤��
��һ�֣��Ƶ�һʢˮ���ձ�������Ϊm1 g����ȡm g��Ͷ���ձ��У���Ӧ�������ȡ�ձ���Һ���������Ϊm2 g���ݴ��Ʋ�������ƵĻ��ϼ�Ϊ+n�ۡ�
�ڶ��֣��ڵ�һ�ַ���������Һ�мӹ���CuSO4��Һ�����ˡ�ϴ�ӡ����������������Ϊm2 g���ݴ��Ʋ�������ƵĻ��ϼ�Ϊ+n�ۡ�
���г������ַ�������ѧ����ʽ��
�ο��𰸣���һ�� m2��m1��(23��n)��23��m?�ڶ���m2�� m/23��n��1/2��98
�������������ˮ��Ӧ����OH������ͨ����Ӧ����Һʹ��ɫ��̪���֤����������H2��ͨ���ռ���ȼ�õ�֤���������ֶ��Ƕ��Եķ�������ֻ��֤�������������ʣ�������˵���ж����������ʡ�Ҫ֤���Ʒ�Ӧ���������Na+����һ����ԭ��ֻʧȥһ�����ӣ�����漰�������Ĺ�ϵ��ֻ��ͨ��������ʵ�飬���ܵ���������ʵ�֡���һ�ַ����У�����������ˮ��ӦʱҺ�������IJ������Ƽ�̬�Ĺ�ϵ����23g����ˮ��Ӧʱ��������+n�������ӣ���Һ������(23��n) g��m g��ʹҺ������(23��n)��23��m g���ڶ��ַ����У�����������ˮ��Ӧ������OH��ȥ����Cu2+���������Ƽ�̬�Ĺ�ϵ����23g����ˮ��Ӧʱ��������+n�������ӣ�������17n g OH����������Cu(OH)2����Ϊ17n��(2��17)��98g��mg�Ʒ�Ӧ���յ�Cu(OH)2����Ϊm/23��n��1/2��98g��
�����Ѷȣ���
2��ѡ���� ��������ˮ�����з�̪��Һ����Ӧ��ʵ�������ܵó��Ľ�����?��?��
A���Ƶ��ܶȱ�ˮС
B���Ƶ�Ӳ��С
C���ƺܻ��ã�����ˮ��Ӧ���ɼ�������
D���Ƶ��۵��
�ο��𰸣�B
�����������
�����Ѷȣ���
3��ѡ���� ����˵����ȷ���ǣ�?��
A��Na2CO3��NaHCO3���ܽ��С
B��������ͬ��Na2CO3��NaHCO3���������ᷴӦ�����ɵ�����CO2
C��ʯ��ˮ�ɼ���Na2CO3��NaHCO3��Һ
D��Na2CO3��NaHCO3ͬʱ������������ȣ�������ȵ����ᷴӦ�����߷ų������
�ο��𰸣�D
���������A����ͬ���¶��£�̼���Ƶ��ܽ�ȴ���̼�����Ƶģ�A����;Bֱ�����û�ѧ����ʽ���м��㣬����Na2CO3��NaHCO3��������Ϊ1g����
��1��Na2CO3�����������ᷴӦ�����ɵĶ�����̼���������Ϊx��
Na2CO3+2HCl�T2NaCl+H2O+CO2��
106? 44
1g? x
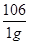 ��
��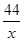
x=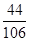 g
g
��1��NaHCO3�����������ᷴӦ�����ɵĶ�����̼���������Ϊy��
NaHCO3+2HCl�T2KCl+H2O+CO2��
84? 44
1g? y
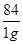 ��
��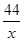
x=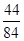 g
g
C����������ʯ��ˮ��Na2CO3��Һ��NaHCO3��Һ��������CaCO3��������������������Һ��C����
D����������ʵ���Ũ����ȣ��ֱ�μ�HCl��Һ����Ӧ���ӷ���ʽΪCO32��+2H���TCO2��+H2O��HCO3��+H���TH2O+CO2������ͬ������NaHCO3��Na2CO3��Ӧ�ų�������ң�NaHCO3��Ӧ���ʿ죬D��ȷ��ѡD��
�����Ѷȣ�һ��
4��ѡ���� ����﮵Ľṹ�������жϴ������
����ˮ��Ӧ���ƾ���?��ԭ�Ӱ뾶С����?����Li2O��Li2O2����������
�������������������������Ƶ���������ͬ?�����ǻ�ԭ��
A���ۢ�
B���٢ڢ�
C���٢ۢ�
D���٢�
�ο��𰸣�C
����������ٴ���﮵Ľ����Ա���������ˮ��Ӧ�Ƹ����ң�����ȷ��ͬ����Ԫ�ش��ϵ��£�ԭ�Ӱ뾶�����۴�����Li2O2������ܴ�������������ֻ��2�����ӣ����Ƶ��������������10�����ӣ������������������������Ƶ������Ӳ���ͬ������ȷ��﮵������ֻ��һ�����ӣ���ʧȥ���ӣ��ǻ�ԭ����
�����Ѷȣ�һ��
5��ѡ����
A��42��53
B��53��42
C��26.5��42
D��42��26.5
�ο��𰸣�C
�����������2NaHCO3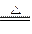 Na2CO3��CO2����H2O֪����NaHCO3���Ȳ���11g CO2ʱ��֪n(NaHCO3)=0.25mol�����ɵ�n(Na2CO3)= 0.25mol����0.25mol Na2CO3���������ᷴӦʱ���ܲ���11g CO2����ԭ�������Na2CO3��NaHCO3�����ʵ�������0.25mol����������Ϊ26.5��42��
Na2CO3��CO2����H2O֪����NaHCO3���Ȳ���11g CO2ʱ��֪n(NaHCO3)=0.25mol�����ɵ�n(Na2CO3)= 0.25mol����0.25mol Na2CO3���������ᷴӦʱ���ܲ���11g CO2����ԭ�������Na2CO3��NaHCO3�����ʵ�������0.25mol����������Ϊ26.5��42��
�����Ѷȣ���