1、选择题 已知aAn+、bB(n+1)+、cCn-、D(n+1)-均具有相同的电子层结构,关于A、B、C、D四种元素的叙述正确的是(? )
A.原子半径:A>B>C>D
B. 原子序数:b>a>c>d
C.离子半径:D>C>B>A
D.金属性:B>A;非金属性:D>C
参考答案:B
本题解析:由已知,A、B为金属,C、D为非金属,由于离子的电子层结构相同,原子序数的关系为:b>a>c>d;离子半径:D>C>A>B;金属性:A>B,非金属性C>D。
本题难度:简单
2、选择题 已知含氧酸可用通式 (OH)nXOm来表示,如X是S,则m=2,n=2,则这个式子就表示H2SO4。一般而言,该式中m大的是强酸,m小的是弱酸。下列各含氧酸中酸性最强的是
A.H2SeO3
B.HMnO4
C.H3BO3
D.H3PO4
参考答案:B
本题解析:选项ABCD中m分别是1、3、0、1,所以答案选B。
本题难度:简单
3、选择题 下列叙述中错误的是?
A.还原性:Na>Mg>Al
B.原子半径:Cl>Si>O
C.稳定性:HF>HCl>HBr
D.酸性:HClO4>H2SO4>H2CO3
参考答案:B
本题解析:A 正确,金属性越强,还原性越强
B 错误,原子半径: Si >Cl>O
C 正确,半径越小越稳定
D 正确,非金属性越强,最高价含氧酸的酸性越强
本题难度:简单
4、填空题 下表为元素周期表的一部分,请回答有关问题:
?
| ⅠA
| ⅡA
| ⅢA
| ⅣA
| ⅤA
| ⅥA
| ⅦA
| 0
|
2
| ?
| ?
| ?
| ?
| ①
| ?
| ②
| ?
|
3
| ?
| ③
| ④
| ⑤
| ?
| ⑥
| ⑦
| ⑧
|
4
| ⑨
| ?
| ?
| ?
| ?
| ?
| ⑩
| ?
|
?
(1)⑤和⑧的元素符号分别是__________和__________。
(2)表中最活泼的金属是__________,非金属性最强的元素是__________。(填写元素符号)
(3)表中能形成两性氢氧化物的元素是__________,分别写出该元素的氢氧化物与⑥和⑨最高价氧化物的水化物反应的化学方程式:______________________________, ________________________________。
(4)请设计一个实验,比较⑦⑩单质氧化性的强弱:
_________________________________________________________________。
参考答案:(1)Si Ar (2)K F
(3)Al 2Al(OH)3+3H2SO4=Al2(SO4)3+6H2O
Al(OH)3+KOH=KAlO2+2H2O
(4)取无色溴化钠的水溶液少许,加入新制氯水,溶液变橙黄色
本题解析:根据周期表中元素的位置可以确定各种元素,如下表所示:
?
ⅠA
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
0
2
?
?
?
?
①N
?
②F
?
3
?
③Mg
④Al
⑤Si
?
⑥S
⑦Cl
⑧Ar
4
⑨K
?
?
?
?
?
⑩Br
?
本题难度:一般
5、计算题 (7分)已知A、B、C、D、E是短周期中的五种非金属元素,它们的原子序数依次增大。A元素原子形成的离子就是一个质子,C、D在元素周期表中处于相邻的位置,B原子的最外层电子数是内层电子数的2倍。E元素与D元素同主族;E的单质为黄色晶体,易溶入CS2
(1)请写出元素符号:B??;C??;
(2)画出E的阴离子结构示意图:?;
(3)A单质和C单质在一定条件下反应生成化合物X,该反应的化学方程式为
?;
(4)将9gB单质在足量的D单质中燃烧,所得气体通入1L 1mol/L的NaOH溶液中,完
全吸收后,溶液中(除Na+外)浓度最大的离子是?。
参考答案:(1) C? N?
(2)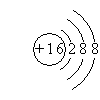
(3)N2+3H2  ?2NH3(2分)
?2NH3(2分)
(4)HCO3―(方程式2分,其余每空1分)
本题解析:略
本题难度:简单