1、选择题 如图是电解CuCl2溶液的装置,其中c、d为石墨电极.则下列有关的判断正确的是( )
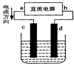
A.a为负极、b为正极
B.d为阳极,电极反应为:2Cl--2e-=Cl2↑
C.电解过程中,d电极质量增加
D.电解过程中,氯离子浓度不变
参考答案:在电解池中,电流的流向和电子的移动方向相反,电流是从正极流向阳极,所以c是阳极,d是阴极,a是正极,b是负极.
A、a是正极,b是负极,故A错误;
B、电解池中,电流是从正极流向阳极,所以c是阳极,d是阴极,阴极上铜离子得电子生成铜,故B错误;
C、电解过程中,d电极是阴极,该电极上铜离子得电子析出金属铜,电极质量增加,故C正确;
D、电解过程中,氯离子在阳极上失电子产生氯气,氯离子浓度减小,故D错误.
故选C.
本题解析:
本题难度:一般
2、选择题 如图所示,将铁棒和石墨棒插入1 L 1 mol/L食盐水中。下列说法正确的是

[? ]
A.若开关K与N连接,铁被保护不会腐蚀
B.若开关K与N连接,正极反应式是4OH- - 4e- = 2H2O+O2↑
C.若开关K与M连接,将石墨棒换成铜棒,可实现铁棒上镀铜
D.若开关K与M连接,当两极共产生28 L(标准状况)气体时,生成了1 mol NaOH
参考答案:D
本题解析:
本题难度:一般
3、选择题 加碘食盐中含有碘酸钾(KIO3),现以电解法制备碘酸钾,实验装置如图所示。先将一定量的碘溶于过量氢氧化钾溶液,发生反应:3I2+6KOH=5KI+KIO3+3H2O,将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区,开始电解。下列说法正确的是
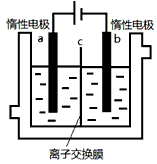
[? ]
A.a电极是阴极
B.a极区的KI最终转变为KIO3
C.阳极电极反应:4OH--4e-==2H2O+O2↑
D.电解过程中OH-从a极区通过离子交换膜c进入b极区
参考答案:B
本题解析:
本题难度:一般
4、选择题 电解尿素[ CO(NH2)2]的碱性溶液制氢的装置示意图如图(电解池中隔膜仅阻止气体通过,a、b极均为惰性电极)。下列说法正确的是
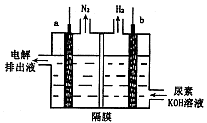
A.电解时,b极是阴极放出H2,发生氧化反应
B.溶液中OH―逐渐向b极移动
C.电解时,a极的电极反应式为: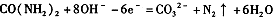
D.若在b极产生标况下224mL氢气,则消耗尿素2g
参考答案:C
本题解析:A中电解时,b极是阴极放出H2,发生还原反应,错误;B中溶液中OH―逐渐向阳极a极移动,错误;C正确;D由电子守恒得:CO(NH2)2~3H2,生成H2 0.01mol,则消耗尿素0.01/3 mol,为0.2g,错误。
本题难度:一般
5、选择题 在1LK2SO4和CuSO4的混合溶液中,c(SO42-)=2.0mol?L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L(标况)气体,则原溶液中K+的物质的量浓度为( )
A.2.0mol?L-1
B.1.5mol?L-1
C.1.0mol?L-1
D.0.5mol?L-1
参考答案:电解1LK2SO4和CuSO4的混合溶液,阳极发生的反应为:4OH-→2H2O+O2↑+4e-,阴极上发生的电极反应为:Cu2++2e-→Cu,2H++2e-→H2↑,两极均收集到22.4L(标况)气体,即均生成1mol的气体,阳极生成1mol氧气说明转移了4mol电子,而阴极上生成的1molH2只得到了2mol电子,所以剩余2mol电子由铜离子获得,且溶液中有1mol铜离子,再根据溶液为电中性,遵循电荷守恒可得钾离子物质的量为2×2-1×2=2mol,所以浓度为2mol/L.
故选A.
本题解析:
本题难度:简单