1、选择题 Cu2O是一种半导体材料,用作制造整流器的材料,还可以用于制船底防污漆(杀死低级海生动物)、农 作物的杀菌剂。在实验室里可模拟工业过程制取Cu2O,总反应式是2Cu+H2O Cu2O+H2↑,其装置如图,下列有关说法不正确的是
Cu2O+H2↑,其装置如图,下列有关说法不正确的是
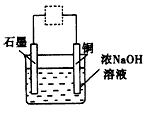
[? ]
A.该实验符合绿色化学的设计理念
B.图中的虚线框内需连接直流电源,且正极与石墨相连
C.CuO高温加热分解也可以得到Cu2O
D.上述装置中,阳极的电极反应式是2Cu+2OH-- 2e-=Cu2O+H2O
参考答案:B
本题解析:
本题难度:一般
2、填空题 (10分)二氧化锰是化学工业中常用的氧化剂和有机合成中的催化剂,其主要制备方法是碳酸锰热分解,反应原理为2MnCO3+O2 2MnO2+2CO2。经研究发现该反应过程为①MnCO3
2MnO2+2CO2。经研究发现该反应过程为①MnCO3 MnO+CO2 ②2MnO+O2
MnO+CO2 ②2MnO+O2 2MnO2。
2MnO2。
回答下列问题:
(1)某温度下该平衡体系的压强为P,CO2、O2的物质的量分别为n1和n2,用平衡分压代替平衡浓度,写出碳酸锰热分解反应的平衡常数表达式K= (分压=总压×物质的量分数);K与反应①、②的平衡常数K1、K2关系为 。
(2)反应②在低温下能自发进行,则其△H 0(填“>”、“<”、“=”)。
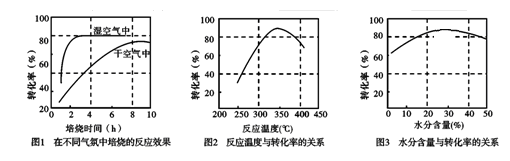
(3)某科研小组对碳酸锰热分解法制二氧化锰的条件(焙烧温度和气氛)进行了研究,获得如下三幅图。该制备反应合适的焙烧温度为 ,合适的含水量气氛条件为 。
(4)MnO2也可在MnSO4―H2SO4―H2O为体系的电解液中电解获得,其阳极的电极反应式为 ,电解后溶液的pH将 (填“增大”、“ 减小”或“不变”)。
参考答案:(1)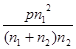 (2分)
(2分) 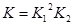 (2分)
(2分)
(2)< (1分) (3)350℃ (1分) 含水量30% (1分)
(4)Mn2+-2e-+2H2O = MnO2+4H+ (2分) 减小(1分)
本题解析:(1)根据题意和题给反应方程式知,碳酸锰热分解反应的平衡常数表达式K=P2(CO2)/P(O2)= 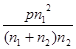 ;K1= P(CO2)、K2=1/P(O2),K与K1、K2关系为
;K1= P(CO2)、K2=1/P(O2),K与K1、K2关系为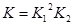 。(2)当△H―T△S<0时反应自发进行,反应②为气体物质的量减少的熵减反应,△S<0,且在低温下能自发进行,则其△H<0。(3)根据图1知,反应在湿空气中进行反应速率快,碳酸锰的转化率高;根据图2知,反应在350℃时碳酸锰的转化率最高,根据图3知,水分含量为30%时碳酸锰的转化率最高,该制备反应合适的焙烧温度为350℃,合适的含水量气氛条件为含水量30% 。(4)电解法制备MnO2阳极发生氧化反应,MnSO4被氧化为MnO2,根据电荷守恒和溶液的酸碱性知,其阳极的电极反应式为Mn2+-2e-+2H2O = MnO2+4H+,阴极发生还原反应,电极反应式为2H++2e-
。(2)当△H―T△S<0时反应自发进行,反应②为气体物质的量减少的熵减反应,△S<0,且在低温下能自发进行,则其△H<0。(3)根据图1知,反应在湿空气中进行反应速率快,碳酸锰的转化率高;根据图2知,反应在350℃时碳酸锰的转化率最高,根据图3知,水分含量为30%时碳酸锰的转化率最高,该制备反应合适的焙烧温度为350℃,合适的含水量气氛条件为含水量30% 。(4)电解法制备MnO2阳极发生氧化反应,MnSO4被氧化为MnO2,根据电荷守恒和溶液的酸碱性知,其阳极的电极反应式为Mn2+-2e-+2H2O = MnO2+4H+,阴极发生还原反应,电极反应式为2H++2e- H2,电解总反应为Mn2+-+2H2O
H2,电解总反应为Mn2+-+2H2O 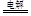 MnO2+ H2+2H+,电解后溶液的pH将减小。
MnO2+ H2+2H+,电解后溶液的pH将减小。
考点:考查化学平衡常数表达式书写,化学反应方向,平衡图像分析和电解原理。
本题难度:困难
3、选择题 下列叙述正确的是( )
A.不溶性盐都是弱电解质,可溶性酸都是强电解质
B.强酸溶液中的氢离子浓度一定大于弱酸溶液中的氢离子浓度
C.二氧化硫和乙醇均属共价化合物,是非电解质
D.NaOH溶液的导电性一定比氨水溶液的导电性强
参考答案:C
本题解析:略
本题难度:简单
4、计算题 (12分)在25 ℃时,用石墨电极电解2.0 L,2.5 mol/LCuSO4溶液。5 min后,在一个石墨电极上有6.4 g Cu生成。试回答下列问题:
(1)有多少摩尔电子发生转移,得到O2的体积(标准状况)是多少升?
(2)溶液的pH是多少?
(3)如用等质量的两块铜片代替石墨作电极,电解后两铜片的质量相差多少?
参考答案:(12分)(1)0.2mol? 1.12L?(2)1?(3)12.8g
本题解析:略
本题难度:一般
5、填空题 如图为持续电解含有一定量CaCl2水溶液(含酚酞)的装置(以铂为电极),A为电流表。电解一段时间t1后,将CO2连续通入电解液中。
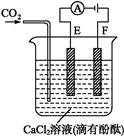
(1)电解时,F极发生 反应,电极反应为 ,E极发生 反应,电极反应为 ,电解总反应为 。
(2)电解池中产生的现象:
① 。
② 。
③ 。
参考答案: (1)氧化 2Cl--2e- Cl2↑ 还原 2H++2e-
Cl2↑ 还原 2H++2e- H2↑ 2Cl-+2H2O
H2↑ 2Cl-+2H2O 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
(2)①通电后E极处溶液呈红色 ②通电时,E极、F极均有气体生成 ③通入CO2时,溶液中先出现白色沉淀,继续通入CO2沉淀又消失
本题解析:溶液中含有:Ca2+、H+、Cl-、OH-,通电时,Ca2+、H+移向阴极,H+放电能力比Ca2+强,在E极上发生反应:2H++2e- H2↑,H2O电离出的H+放电,OH-富集在阴极(E极),则使阴极区溶液变红;Cl-、OH-移向阳极,Cl-在阳极放电,2Cl-
H2↑,H2O电离出的H+放电,OH-富集在阴极(E极),则使阴极区溶液变红;Cl-、OH-移向阳极,Cl-在阳极放电,2Cl- Cl2↑+2e-,总反应方程式:2Cl-+2H2O
Cl2↑+2e-,总反应方程式:2Cl-+2H2O Cl2↑+H2↑+2OH-;电解一段时间t1后,溶液中OH-浓度增大,相当于Ca(OH)2、CaCl2的混合溶液,通入CO2:Ca2++2OH-+CO2
Cl2↑+H2↑+2OH-;电解一段时间t1后,溶液中OH-浓度增大,相当于Ca(OH)2、CaCl2的混合溶液,通入CO2:Ca2++2OH-+CO2 CaCO3↓+H2O,继续通入CO2:CaCO3+CO2+H2O
CaCO3↓+H2O,继续通入CO2:CaCO3+CO2+H2O Ca(HCO3)2。
Ca(HCO3)2。
考点:电解原理
本题难度:一般