1、选择题 关于化学键的下列叙述中,正确的是
[? ]
A.离子化合物中只含离子键
B.共价化合物中只含非金属元素
C.离子化合物中可能含共价键
D.离子化合物中一定含有金属离子
2、填空题 (4分)下面是你熟悉的物质:
①O2② 金刚石 ③ NaBr ④ H2SO4⑤ Na2CO3⑥ K2S?⑦NaHSO4
小题1:这些物质中,只含共价键的是_______________;只含离子键的是___________;既含共价键又含离子键的是_______________。
小题2:将NaHSO4溶于水,写出其电离方程式______________________________。
3、填空题 具有光、电、磁等特殊功能的新型材料是目前化学研究的热点之一,二硫醇烯与锌的配合物(C)的一种合成途径如下。
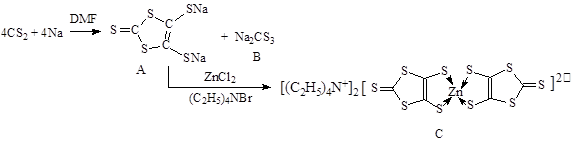
(1)锌原子基态时核外电子排布式为?。
(2)下列说法正确的是?(不定项选择)。
a.金属钠的熔点比金属锂高
b.金属钠晶体属于面心立方堆积
c.CS2的沸点比CO2高
d.硫化钠晶胞(如图所示)中含4个S2-离子
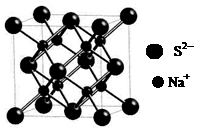
(3)化合物B中CS32-的空间构型是?(用文字描述)
(4)配合物C中Zn2+的配位数是?(填数字),N原子杂化方式是?。
(5)1mol化合物A中含有σ键的数目为?。
4、填空题 如图中A、B、C、D是同周期或同主族的相邻元素:
①已知:A元素的最低价为-3价,它的最高价氧化物含氧56.34%,原子核内中子数比质子数多1个,则A元素原子质量数为______,原子序数为______,A元素位于第______周期______族.
②写出元素符号A:______,B:______,C:______,D:______.
③A、B、C三种元素最高价氧化物的水化物的化学式依次为______,______,______,其中酸性最强的是______.
④B、D两种元素和氢组成的气态氢化物的化学式依次为______,______其中______稳定性最大,______还原性最强.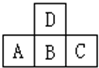
5、填空题 (15分)(物质结构与性质)CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。已知 :
:
①CuCl可以由CuCl2用适当的还原剂如SO2、SnCl2等还原制得:
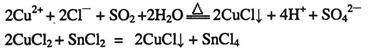
②CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子:

请回答下列问题:
(1)基态Cu原子的核外电子排布式为?。H、N、O三种元素的电负性由大到小的顺序是? ?。
?。
(2)SO2分子的空间构型为____________。与SnCl4互为等电子体的一种离子的化学式为
?。
(3)乙二胺分子 中氮原子轨道的杂化类型为?。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是_?。
中氮原子轨道的杂化类型为?。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是_?。
(4)②中所形成的配离子中含有的化学键类型有_______。(填字母)
a.配位键? b.极性键? c.离子键? d.非极性键
(5)CuCl的晶胞结构如右图所示,其中Cl原子的配位数为_____。