1������� (14��)�� NH4Cl��������ʵ�飬���жϷ�����������˵��ԭ��
(1)�ò�����պȡ���� NH4Cl��Һ��pH��ֽ�Ӵ�ʱ����ֽ��ʾ����ɫ�����ɫ����ȣ��ɷ��� NH4Cl��pH ?7(�<������=����>��������?�ԣ���ᡱ��������С�������ԭ��������ӷ���ʽ��ʾΪ?��
(2)��NH4Cl��Һ�м���þ�ۣ��ɹ۲쵽���������ɣ�����Ҫ�ɷ�Ϊ??��
(3)����NH4Cl��Һ���вⶨ����Һ��Ũ��������?���ӣ����������ٵ���?���ӡ�
��4��25��ʱ����0.1mol/L�İ�ˮ�м��������Ȼ�粒��壬�������ܽ�����ҺpH��С����Ҫԭ���ǣ�����ţ�?��
A����ˮ���Ȼ�立�����ѧ��Ӧ
B���Ȼ����Һˮ�������ԣ�������c(H+)
C���Ȼ������ˮ���������������ӣ������˰�ˮ�ĵ��룬ʹc(OH�D)��С
��5�������£������0.1mol NH4Cl��0.05mol NaOHȫ������ˮ���γɻ����Һ(��������ʧ)��
��?��?�������ӵ����ʵ���֮�͵���0.1mol��
��_?__��_?�������ӵ����ʵ���֮�ͱ�OH�D��0.05mol��
2��ѡ����
L��1 CH3COOHˮ��Һ����50 mL 0.20��mol��L��1����ˮ��Һ�����ϸ�ƿ��Һ�������ӡ����������Ĵ�С˳����
A���٣��ڣ��ۣ��ܣ���
B���ڣ��٣��ۣ��ܣ���
C���ڣ��ۣ��ܣ��٣���
D���ݣ��ܣ��ۣ��ڣ���
3��ѡ���� ���в����Եζ������Ӱ����ǣ�?��
A��ʢ����Һ����ƿ���ô���Һ��ϴ
B���ζ��ܼ��첿�������ݣ��ζ�������������ʧ
C���ζ����ڵζ�ǰҺ����0�̶�����
D���ﵽ�ζ��յ�ʱ���Ӷ�ȡ�ζ�����Һ�����
4��ʵ���� ���������Ʒ�� NH4ClO4�ĺ������������вⶨ������װ����ͼ��ʾ(���Ⱥ������̶�װ������ȥ)��ʵ�鲽�����£�
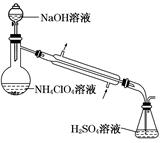
���� 1������ͼ��ʾ��װ���������װ�������ԡ�
���� 2��ȷ��ȡ��Ʒa g (Լ 0.5 g)��������ƿ�У�����Լ 150 mL ˮ�ܽ⡣
���� 3��ȷ��ȡ 40.00 mL Լ 0.1 mol��L��1 H2SO4��Һ����ƿ�С�
���� 4������Һ©����������ƿ�м��� 20 mL 3 mol��L��1NaOH ��Һ��
���� 5������������������ƿ��ʣ��Լ 100 mL ��Һ��
���� 6��������й���ˮ��ϴ����װ�� 2��3 �Σ�ϴ��Һ������ƿ�С�
���� 7������ƿ�м������ָʾ������ c mol��L��1NaOH ����Һ�ζ����յ㣬���� NaOH ����Һ V1 mL��
���� 8����ʵ�鲽�� 1��7 �ظ� 2 �Ρ�
�ٲ��� 3�У�ȷ��ȡ 40.00 mL? H2SO4��Һ�IJ���������?��
�ڲ��� 1��7 �У�ȷ�����ɵİ���ϡ������ȫ���յ�ʵ�鲽����?(������)��
��Ϊ�����Ʒ�� NH4ClO4�ĺ��������貹���ʵ����?��
5������� ϡ��ˮ�д�������ƽ�⣺NH3��H2O NH3��H2O
NH3��H2O NH4+��OH��
NH4+��OH��
��֪��25��ʱ��Һ�д������й�ϵ��K��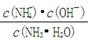 ��1.8��10-5
��1.8��10-5
��1����ϡ��ˮ��ͨ�백��ʱ��ƽ����?�ƶ����á��ҡ���������գ���ͬ������ϡ��ˮ�м�����������ʱ��ƽ����?�ƶ���
��2������ˮ�м���ϡ���ᣬʹ��ǡ����ȫ�кͣ�������ҺpH?7����������������������������ӷ���ʽ��ʾ��ԭ��?������ˮ�м�������(NH4)2SO4���壬��ʱ��Һ��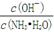 ?�����������С�����䡱����
?�����������С�����䡱����
��3��25��ʱ������ˮ����ʼŨ��Ϊ0.5?mol/L��ƽ��ʱ��Һ��c(OH��)��__________________��pH��______����ˮ�м���ϡ��������Һ��pH��7ʱ��c(NH4+)��a mol��L��1���ٶ�HSO4����ȫ���룬����Һ��c(SO42��)��?��