1、填空题 (10分)已知T、X、Y、Z是四种常见的短周期元素,其结构或性质信息如下表。请填空:

(1)写出与Y2互为等电子体的物质的分子式?。
(2)写出Y的最简单气态氢化物的结构式?。
(3)元素Q的原子序数比X与Z的原子序 数之和还多1。
数之和还多1。
①该元素基态原子的价电子排布式为? ?。
?。
②向含Q离子的水溶液中逐滴加入Y的简单氢化物的水溶液至过量,写出有关反应的离子方程式?、?。
参考答案:(每空2分 ,共10分)
,共10分)
(1)CO?(2)NH3的结构式
(3)① 3d104s1
②Cu2++2NH3・H2O=Cu(OH)2↓+2NH4+
Cu(OH)2+4NH3・H2O=[Cu(NH3)4]2++2OH-+4H2O
本题解析:略
本题难度:一般
2、填空题 (15分)
常温下D、E、F、I、J为气体,H、I、J都为氧化物;C的焰色反应为黄色;M为红褐色的固体,由G分解得到的H、I、J三者的物质的量相等.下图表示各物质之间的转化关系.

试回答下列问题:
(1)写出L的化学式?.
(2)基于反应①原理的化学工业称为?.
写出该反应①的离子方程式?.
(3)反应②的现象是?.
(4)写出H与Al在高温下反应的化学方程式?.
(5)写出反应③的化学方程式? ?.
?.
参考答案:
(1)Fe(OH)2(2分)
(2)氯碱工 业(2分)? 2Cl-+2H2O
业(2分)? 2Cl-+2H2O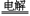 2OH-+H2↑+Cl2↑(3分)
2OH-+H2↑+Cl2↑(3分)
(3)白色→灰绿色→红褐色(2分)
(4)3FeO + 2Al Al2O3 + 3Fe (3分)
Al2O3 + 3Fe (3分)
(5)FeC2O4 FeO + CO↑+CO2↑(3分)
FeO + CO↑+CO2↑(3分)
本题解析:略
本题难度:一般
3、选择题 已知A、B、C是中学化学的常见物质,它们在一定条件下有如下转化关系,下列说法错误的是
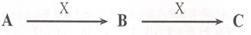
 ?
?
A.若A是一种淡黄色固体,B是造成酸雨的“罪魁祸首”,则X为O2
B.若B与新制氢氧化铜共热,有砖红色沉淀生成,且C能使湿润的蓝色石蕊试纸变红,则A和C可以反应生成酯
C.若B为两性氢氧化物,则C中一定存在Al3+
D.A既可以为金属单质,也可以为非金属单质
参考答案:C
本题解析:略
本题难度:一般
4、填空题 一种以黄铜矿和硫磺为原料制取铜和其他产物的新工艺,原料的综合利用率较高。其主要流程如下:
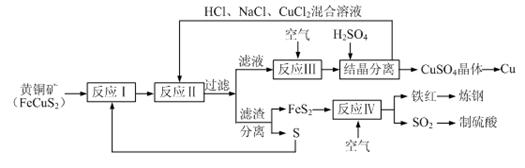
注:反应Ⅱ的离子方程式为Cu2++CuS+4Cl―=2CuCl2-+S
请回答下列问题:
⑴反应Ⅰ的产物为(填化学式)? ▲?。
⑵反应Ⅲ的离子方程式为? ▲?。
⑶一定温度下,在反应Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸铜晶体,其原因是
? ▲?。
⑷炼钢时,可将铁红投入熔融的生铁中,该过程中主要反应的化学方程式是? ▲?。
⑸某硫酸厂为测定反应Ⅳ所得气体中SO2的体积分数,取280mL(已折算成标准状况)气体样品与足量Fe2(SO4)3溶液完全反应后,用浓度为0.02000 mol/L的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00 mL 。
已知:Cr2O72-+ Fe2++ H+→Cr 3++
3++  Fe3++ H2O(未配平)
Fe3++ H2O(未配平)
①SO2通入Fe2(SO4)3溶液,发生反应的离子方程式为? ▲?。
②反应Ⅳ所得气体中SO2的体积分数为? ▲?。
参考答案:⑴FeS2、CuS
⑵4CuCl2-+O2+4H+ =4Cu2++8Cl-+2H2O
=4Cu2++8Cl-+2H2O
⑶该温度下,硫酸铜的溶解度小于氯化铜
⑷3C+Fe2O3 2Fe+3CO
2Fe+3CO
⑸①SO2 + 2Fe3++ 2H2O=SO42-+ 2Fe2++ 4H+? ②12.00% (每空2分,共12分)
本题解析:略
本题难度:一般
5、填空题 (16分)X、Y、Z为常见的三种单质,Z是绿色植物光合作用的产物之一,A、B为常见化合物。它们在一定条件下可发生如图所示的反应(均是在非溶液中进行的反应):
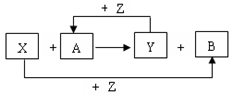
(1)画出Z的原子结构示意图?▲?;
(2)当X为金属,Y为非金属时,A可能的电子式为?▲?或?▲?;
(3)当X为非金属,Y为金属时,X可能的化学式为?▲?或?▲?;
(4)当X与Y均为金属时,写出X与A反应的化学方程式?▲?;
(5)当X与Y均为非金属时,若X与Y同主族,写出X与A反应的化学方程式?▲?;
若X与Y不在同一主族,写出X与A反应的化学方程式?▲??。
参考答案:(1)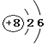
(2)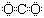 或
或
(3)C或H2
(4)2Al+ Fe2O3? ?2Fe+Al2O3
?2Fe+Al2O3
(5)C+SiO2 ? Si+CO2? C+H2O
? Si+CO2? C+H2O ?H2+CO
?H2+CO
本题解析:分析:先根据C是单质且C是绿色植物光合作用的产物之一,判断C是氧气,A、B是单质,与氧气反应,得出X、Y是含氧化合物,然后采用假设的方法分析.
解析:C是单质且C是绿色植物光合作用的产物之一,所以C是O2.A、B是单质,分别与O2反应生成含氧化合物,A+X→B+Y,属置换反应.
(2)如果X是钠,Y是氢气,A就是H2O,B就是NaOH,钠与水反应的方程式为
2Na+2H2O=2NaOH+H2 ;
(3)当X为非金属,Y为金属时,就是以氢气或一氧化碳为还原剂的热氧化还原反应;
(4)当X与Y均为金属时,考虑铝热反应;
(5) X是碳,Y是硅,A就是SiO2,B就是CO,C与SiO2的反应方程式为:
2C+SiO2 ?Si+2CO↑;如果X是碳,B是氢气,X就是H2O,Y就是CO,C+H2O
?Si+2CO↑;如果X是碳,B是氢气,X就是H2O,Y就是CO,C+H2O ?H2+CO;
?H2+CO;
点评:本题的题眼是:C是单质且C是绿色植物光合作用的产物之一,通过判断A、B、X、Y,确定该反应是置换反应,学过的置换反应方程式较多,考查学生的发散思维以及总结归纳能力.
本题难度:一般