1、填空题 (14分)食盐是日常生活的必需品,也是重要的化工原料。
(1)粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO2-4"等杂质离子,实验室提纯NaCl的流 程如下:
程如下:
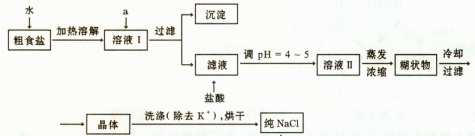
提供的试剂:饱和Na2CO3溶液?饱和K2CO3溶液? NaOH溶液? BaCl2溶液? Ba(NO3)2溶液? 75%乙醇?四氯化碳
①欲除去溶液I中的Ca2+、Mg2+、Fe3+、SO2-4离子,选出a所代表的试剂,按滴加顺序依次为?(填化学式);滤液中滴加盐酸调pH ="4" ~5的目的是?;
②选用75%乙醇洗涤除去NaCl晶体表面附带的少量KCl,检验NaCl是否洗净的操作是?;
(2)用提纯的NaCl配制480mL 4.00mol・L-1NaCl溶液,需要称取的质量为?g,所用仪器除药匙、玻璃棒、烧杯外还有?(填仪 器名称);
器名称);
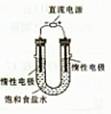
(3)电解饱和食盐水的装置如图所示,若收集的H2为2L,则同样条件下收集的Cl2____(填“>”、“=”或“<”)2L,主要原因是?。
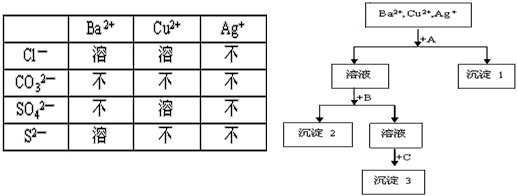
2、推断题 某工业废水中含有Ba2+,Cu2+,Ag+,选择合适试剂,将这三种离子逐一沉淀分离。其流程图如下:
(1)沉淀1的化学式为________________
(2)写出混合液+A的离子方程式_____________________
(3)若C为Na2S;且它与B属于同一类盐,则B试剂的名称是________________
3、选择题 下列物质中所含分子物质的量最多的是
A.56 gN2
B.1.5 molO2
C.标准状态下22.4 LCl2
D.3.01×1023个硫酸分子
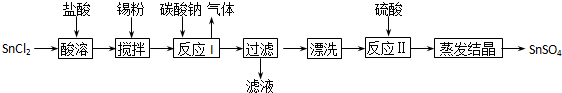
4、填空题 (14分)工业上SnSO4是一种重要的硫酸盐,广泛应用于镀锡工业,其制备路线如下:
提示:①已知在酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式.
②已知Ksp[Sn(OH)2] =1.0×10-26
回答下列问题:
(1)SnCl2用盐酸而不用水直接溶解的原因是__________,加入Sn粉的作用是_________。
(2)反应I生成的沉淀为SnO,写出该反应的离子方程式___________________________。
(3)检验沉淀已经“漂洗”干净的方法__________________________________________。
(4)反应Ⅱ硫酸的作用之一是控制溶液的pH,若溶液中c(Sn2+)=1.0mol?L-1,则应控制溶液pH_____。
(5)酸性条件下,SnSO4还可以用作双氧水去除剂,请写出发生反应的离子方程式____________。
5、选择题 0.1?mol/L?Na2SO4的溶液中Na+的物质的量浓度
A.0.1mol/L
B.0.2 mol/L
C.0.01 mol/L
D.0.02 mol/L