1、填空题 (15分)
M、Q、X、Y、Z是前四周期的5种元素,原子序数依次增大,其结构或性质信息如下表:
元素
| 结构或性质信息
|
M
| M的一种单质是自然界最硬的物质
|
Q
| 基态原子最外层未成对电子数在该元素所在周期中最多
|
Y
| 单质常温、常压下是气体。基态原子的M层上有1个未成对的p电子
|
?请回答以下问题:
(1)a.学生甲根据M原子易形成4对共用电子的特点,推出M原子应该具有4个未成对电子。画出基态M原子的价层电子排布图为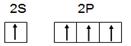 ,请判断对错,并加以解释?
,请判断对错,并加以解释?
b.M的另一种单质被称为混合型晶体,具有平面层状结构。M原子的杂化方式为________,其晶体中含有的作用力为________________________________________
(2)写出与Q单质分子互为等电子体的常见微粒的化学式(分子、阴离子各1个)?、?;并写出该阴离子的 电子式___________
电子式___________
(3)a.学生乙通过查表,确定Q与Y的电负性接近。但是Q的氢化物分子间能形成氢键,X的氢化物分子间却不易形成氢键,试从结构的角度加以解释:?
b.氢键的形成,对分子的沸点影响较大,请判断以下两种互为同分异构体的分子沸点高低:
邻羟基苯甲酸 ______ 对羟基苯甲酸,原因是_________________________________
c.含氧酸的酸性与非羟基氧的个数有关,则Y的四种常见的不同价态含氧酸的酸性由强到弱排序为:?
2、选择题 由短周期元素和长周期元素共同组成的族可能是
A.主族
B.副族
C.Ⅷ族
D.Ⅶ族
3、选择题 短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法正确的是(?)
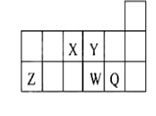
A.第一电离能和电负性: Z>W>Q
B.元素W的最高价氧化物对应的水化物的酸性比Q的强
C.离子半径X3-<Z 3+
D.元素X与元素Q二者的氢化物能化合生成离子化合物
4、选择题 元素R有如下反应:RO3―+5R-+6H+===3R2+3H2O,下列说法正确的是(?)
A.元素R位于周期表中第ⅤA族
B.RO3―中的R只能被还原
C.每反应消耗1 mol RO3―,转移电子的物质的量为5 mol
D.R2在常温常压下一定是气体
5、填空题 周期表中前36号元素A、B、C、D、E、F、G、H,它们的原子序数依次增大,其中B、C、D为同一周期;E、F、G为同一周期;A和E、D和G分别为同一主族;A与B组成的化合物是一种温室气体;D元素原子的最外层电子数是次外层电子数的3倍;E是所在周期原子半径最大的元素(除稀有气体外);F元素的离子半径是同周期元素形成的简单离子中最小的;H元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子。
(1)E2D2物质中化学键的类型是__________________
(2)一定条件下,A2气体与C2气体充分反应可生成6.8 g的气体,放出18.44 kJ热量,则该反应的热化学方程式为:_________________________________________;生成物分子的空间构型为_________________,其中C的杂化方式为_______________。
(3)C和E组成的一种离子化合物,能与水反应生成两种碱,该反应的化学方程式是
?。
(4)H的基态原子的电子排布式为__________________________已知H2+能与(2)中的生成物的水溶液形成配合物,请写出该配合物中阳离子的结构简式:_________________,在此配合物的水溶液中加入乙醇,现象是_______________________________________。
(5)将足量的GD2通入EDA溶液中所得溶液的离子浓度的大小顺序为:?