1������� �����ŷ�CO2����ɡ�����ЧӦ������ѧ�������о���ν�CO2ת��Ϊ�����õ���Դ������һ�ַ������ǽ�CO2ת��Ϊ������ȼ�ϼ״���CH3OH�����仯ѧ����ʽΪ��

����գ�
��1��д��������Ӧ��ƽ�ⳣ������ʽ______��
��2�����ݻ�Ϊ2L���ܱ������У���һ�����Ķ�����̼��һ����������һ�������ºϳɼ״���ʵ������ͼ��ʾ������˵����ȷ����______������ţ�
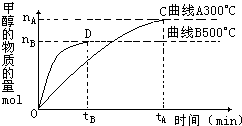
A����300�棬�ӷ�Ӧ��ʼ��ƽ�⣬�״���ƽ����Ӧ����v��CH3OH��=
mol?��L?min��-1
B����Ӧ��ϵ��300�����µ�500�棬ƽ�ⳣ��K�仯��
C���÷�Ӧ������ӦΪ���ȷ�Ӧ
D������C��ķ�Ӧ��ϵ��300�����ߵ�500�棬����
��3��25�棬1.01��105Paʱ��16g?Һ̬�״���ȫȼ�գ����ָ���ԭ״̬ʱ���ų�369.2kJ���������÷�Ӧ���Ȼ�ѧ����ʽΪ��______��
��4��ѡ�ú��ʵĺϽ�Ϊ�缫�����������ơ��״���ˮ������Ϊԭ�ϣ������Ƴ�һ���Լ״�Ϊԭ�ϵ�ȼ�ϵ�أ��˵�صĸ���Ӧ�����ͨ���������______�������ĵ缫��Ӧʽ��______��
�ο��𰸣���1������K=�������Ũ����֮�����Է�Ӧ���Ũ����֮�����ó�K=c(CH3OH)?c(H2O)c(CO2)?c3(H2)���ʴ�Ϊ��K=c(CH3OH)?c(H2O)c(CO2)?c3(H2)��
��2��A����ѧ��Ӧ���ʵ��ڵ�λʱ��������Ũ�ȵı仯�����״���ƽ����Ӧ����v��CH3OH��=nA2tAmol?��L?min��-1����A����
B������ͼʾ��Ϣ�������¶ȣ��״������ʵ������٣����Է�Ӧ������У�����Ӧ�Ƿ��ȷ�Ӧ�����ڷ��ȷ�Ӧ�������¶ȣ�ƽ�ⳣ����С����B����
C������ͼʾ��Ϣ�������¶ȣ��״������ʵ������٣����Է�Ӧ������У�����Ӧ�Ƿ��ȷ�Ӧ����C��ȷ��
D��C��ʱ��Ӧ�ﵽƽ��״̬�������¶ȣ����ڸ÷��ȷ�Ӧ��ƽ��������У�����n(H2)n(CH3OH)����D��ȷ��
��ѡCD��
��3��16g?Һ̬�״���ȫȼ�գ����ָ���ԭ״̬ʱ���ų�369.2kJ����������1mol?Һ̬�״���ȫȼ�գ����ָ���ԭ״̬ʱ���ų�725.8kJ�����������Ȼ�ѧ����ʽΪ��
CH3OH��l��+32?O2=CO2��g��+2H2O��l����H=-725.8kJ/mol���ʴ�Ϊ��CH3OH��l��+32?O2=CO2��g��+2H2O��l����H=-725.8kJ/mol��
��4���״�Ϊԭ�ϵ�ȼ�ϵ���У�ȼ�ϼ״�Ϊ����������ʧ���ӵ�������Ӧ�������������������õ��ӵû�ԭ��Ӧ�����������Լ���ֻ��ѡ����������Ϊ����ʣ��ڼ��Ի����£������ķŵ����Ϊ��O2+2H2O+4e-=4OH-���ʴ�Ϊ���״���O2+2H2O+4e-=4OH-��
���������
�����Ѷȣ�һ��
2��ѡ���� ��25�桢101kPa�£�1g�״�ȼ������CO2��Һ̬ˮʱ����22��68kJ�������Ȼ�ѧ����ʽ��ȷ����
[? ]
A��CH3OH(l)+ 3/2O2(g)==CO2(g)+2H2O(l) ��H=+725��8kJ/mol
B��2CH3OH(l)+3O2(g)==2CO2(g)+4H2O(l) ��H=��1452kJ/mol
C��2CH3OH(l)+3O2(g)==2CO2(g)+4H2O(l) ��H=��725��8kJ/mol
D��2CH3OH(l)+3O2(g)==2CO2(g)+4H2O(l) ��H=+1452kJ/mol
�ο��𰸣�B
���������
�����Ѷȣ���
3��ѡ���� �����Ȼ�ѧ����ʽ��ȷ���ǣ�ע����H�ľ���ֵ����ȷ���� ? ��
A��C2H5OH��l��+3O2��g���T2CO2��g��+3H2O��g����H=-1367.0?kJ/mol��ȼ���ȣ�
B��NaOH��aq��+HCl��aq���TNaCl��aq��+H2O��l����H=-57.3kJ/mol���к��ȣ�
C��S��s��+O2��g���TSO2��g����H=-269.8kJ/mol����Ӧ�ȣ�
D��2NO2�TO2+2NO��H=+116.2kJ/mol����Ӧ�ȣ�
�ο��𰸣�BC
���������
�����Ѷȣ�һ��
4�������
��.�������(K2FeO4)�Ǽ��õ������������и�Ч���������ã�Ϊһ�����ͷ��ȸ�Ч�������������������������£�
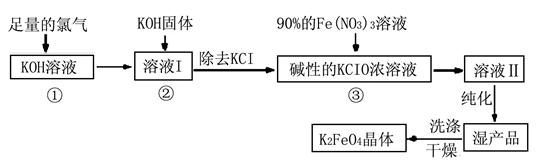
��ͬ���������⡣
��1��д����KOH��Һ��ͨ������Cl2������Ӧ�����ӷ���ʽ ��
��2������ҺI�м���KOH�����Ŀ���� (ѡ�����)��
A��Ϊ��һ����Ӧ�ṩ���ԵĻ���
B��ʹKClO3ת��ΪKClO
C������ҺI�й�����Cl2������Ӧ�����ɸ����KClO
D��KOH�����ܽ��ų��϶����������������߷�Ӧ���ʺ�KClO�Ĵ���
 3Zn+2K2FeO4+8H2O��
3Zn+2K2FeO4+8H2O��