| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点归纳《盐类水解的原理》考点强化练习(2017年押题版)(十)
参考答案:C 本题解析:A.在水溶液中,铵根离子水解而使其溶液呈酸性,硫酸氢铵在电离出氢离子,抑制铵根离子水解,所以物质的量浓度相等的氯化铵和硫酸氢铵溶液中,铵根离子浓度硫酸氢铵大于氯化铵,错误;B.醋酸钠是强碱弱酸盐,醋酸根离子水解,溶液呈碱性,所以c(OH-)>c(H+),所以c(Na+)>c(CH3COO-)>c(OH-)>c(H+),错误;C.碳酸根离子在水溶液里分两步水解,CO32-+H2O 本题难度:一般 2、填空题 现有下列10种物质: |
参考答案:(共14分,每空2分)
(1)⑤(有错计0分) ①②⑥(对两个计1分,全对2分,有错0分)
(2) 碱 HCO3-+H2O  H2CO3+ OH-, HCO3-
H2CO3+ OH-, HCO3- CO32-+H+ 因水解程度大于电离
CO32-+H+ 因水解程度大于电离
程度,所以溶液显碱性(合理答案均可,只要写出水解方程式即计满分)
(3) C (有错0分)
(4) a + b = 14 a > b
本题解析:(1)非电解质是指在熔融状态下或水溶液中不能导电的化合物。故属于非电解质的是⑤。既能跟盐酸反应又能跟NaOH溶液反应的是①②⑥。
(2)NaHCO3是强碱弱酸盐,水解呈碱性,水解的离子方程式为HCO3-+H2O  H2CO3+ OH-, HCO3-
H2CO3+ OH-, HCO3- CO32-+H+。
CO32-+H+。
(3)A项:酸的浓度和碱的浓度一样,Al的质量相同,生成的H2的量也一样,故错。
B项:CH3COOH是弱电解质,部分电离,故溶液中的c(CH3COO-)为原溶液浓度的小于1/2,故错。
D项:CH3COONa是强碱弱酸盐,部分水解,加水稀释促进水解,CH3COOH是弱电解质,部分电离,加水稀释促进电离,故溶液的pH:Ⅳ >Ⅲ>Ⅱ>Ⅰ,故错。
故选C。
(4)HCl是强电解质,全部电离,AlCl3是强酸弱碱盐,发生水解,则则a和b之间满足的关系为a + b = 14 ;a > b。
考点:非电解质的判断 盐类水解
点评:本题重点考查的是非电解质的判断和盐类水解的知识,题目难打较大,注意对基础知识的学习及应用。
本题难度:一般
3、选择题 物质的量浓度相同的下列溶液中,NH4+浓度最大的是
A.NH4Cl
B.NH4HSO4
C.CH3COONH4
D.NH4HCO3
参考答案:B
本题解析:NH4++H2O NH3.H2O+H+,根据化学平衡原理,加入氢离子可以大大抑制铵根离子的水解,所以上述四个选项中,当物质的量浓度相同的下列溶液中,NH4+浓度最大的是NH4HSO4,所以本题的答案为B。
NH3.H2O+H+,根据化学平衡原理,加入氢离子可以大大抑制铵根离子的水解,所以上述四个选项中,当物质的量浓度相同的下列溶液中,NH4+浓度最大的是NH4HSO4,所以本题的答案为B。
考点:盐类水解
点评:本题考查了盐类的水解,该考点是高考考查的重点,本题有一定的综合性,难度失踪。
本题难度:一般
4、填空题 X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。
请回答下列问题:
(1)五种元素原子半径由大到小的顺序是(写元素符号)________。
(2)由以上某些元素组成的化合物A、B、C、D有如下转化关系:
A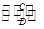 B(在水溶液中进行)
B(在水溶液中进行)
其中C是溶于水显酸性的气体;D是淡黄色固体。
写出C的结构式________;D的电子式________。
①如果A、B均由三种元素组成,B 为两性不溶物,则A的化学式为____________;由A转化为B的离子方程式为_____________________________________________。
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。用离子方程式表示A溶液显碱性的原因:________________________________________。A、B浓度均为0.1 mol・L-1的混合溶液中,离子浓度由大到小的顺序是__________________;常温下,在该溶液中滴加稀盐酸至中性时,溶质的主要成分有_______________________________。
参考答案:(1)Na>Al>C>O>H
(2)O=C=O Na+[∶O∶,∶∶O∶,∶∶]2-Na+
①NaAlO2 AlO2-+2H2O+CO2=Al(OH)3↓+HCO3- (或2AlO2-+3H2O+CO2=2Al(OH)3↓+CO32-)
②CO32-+H2O
本题解析:
本题难度:困难
5、选择题 把0.2mol/L NH4Cl溶液与0.1mol/L NaOH溶液等体积混合后溶液中下列微粒的物质的量浓度的关系正确的是
A.[NH4+]=[Na+]=[OH-]>[NH3・H2O]
B.[NH4+]=[Na+]>[NH3・H2O]>[OH-]
C.[NH4+]>[Na+]>[OH-]>[NH3・H2O]
D.[NH4+]>[Na+]>[NH3・H2O]>[OH-]
参考答案:D
本题解析:此类型题目,若发生化学反应,优先考虑化学反应,通过化学反应各种离子浓度能比较出来,则不必考虑水解和电离,因为弱电解质电离或盐的水解程度都很小,对离子浓度,影响不大,若通过化学反应各种离子浓度大小比较不出来则再考虑水解和弱电解质电离。此题中NH4Cl和NaOH发生反应:NH4Cl+NaOH=NaCl+NH3・H2O生成NH3・H2O,同时NH4+有剩余若不考虑NH3・H2O电离和NH4+水解,有[NH3・H2O]=[NH4+]=[Na+]=0.5mol/L,此时考虑电离和水解: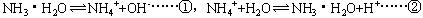
①发生使溶液 [NH4+]增大,②反应使溶液[NH4+]减小,溶液[NH4+]是增大还是减小,取决于两个反应哪一个为主要,根据经验规则可知,盐的水解和弱电解质的电离,以电离为主,因此[NH4+]增大,大于[Na+],同样分别[NH3・H2O]应减少,小于[Na+],溶液中[OH-]来自NH3・H2O电离,电离很微弱,[OH-]浓度很小,故微粒浓度顺序为[NH4+]>[Na+]>[NH3・H2O]>[OH-],选择D。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《物质结构和.. | |