| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《无机综合与推断》考点预测(2017年强化版)(十)
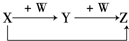 参考答案:A 本题解析: 本题难度:一般 3、填空题 (11分)、A、B、C、D、E为中学化学常见的单质或化合物,相互转化关系如图所示。 参考答案:(11分)、⑴①CO (1分)? ② 4NH3+5O2 本题解析:略 本题难度:一般 4、选择题 由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如 右图转化关系(部分生成物和反应条件略去)。下列推断不正确的是 参考答案:A 本题解析:试题分析:若X是Na2CO3,C为CO2,则B为HCl,D为NaHCO3,A为Cl2,E为HClO,D与E可以发生反应,生成NaClO.因此,选项A说法错误。故答案选A。 本题难度:简单 5、填空题 A、B、C、D、E、F、X存在如图所示转换关系,其中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。X可能是强酸,也可能是强碱。 参考答案:(1)(NH4)2S(2分) (2)Cl2+SO2+2H2O=4H++SO42-+2Cl-(2分) 本题解析: 本题难度:一般 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点归纳《化学常用计.. | |