1������� ��15�֣�������Ԫ�����ڱ���һ���֣����ݸ�����Ԫ�ػش���������
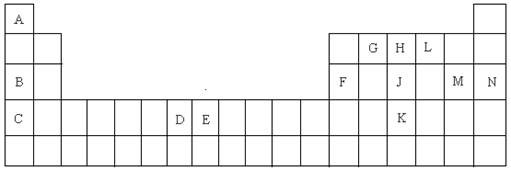
��1��K��Ԫ�ط�����?��
��2��DԪ�ص���Χ�����Ų�ͼ��?�����仯�����У����������?��
��3��CԪ�ص�ԭ�ӽṹʾ��ͼ��?��
��4��A��L��B��L���ֱ����γ�ԭ�Ӹ�����Ϊ1��1�Ļ����A��L��1��1���Ļ�������?���ӣ���Ի�Ǽ��ԣ���B��L��1��1���Ļ�����ĵ���ʽ��?��
��5��G��H��Lԭ�ӵĵ�һ�������ɸߵ��͵�˳����?����Ԫ�ط��ţ���
��6��J���ʵ�һ�ְ�ɫͬ���칹��Ŀռ乹����?��
��7��EԪ����Ԫ�����ڱ��е�λ����?�����仯�����У����У�2����3�۵�2�����ӣ���3�����ӱȽ��ȶ�����ԭ����?��
��8��A��B�Ļ�������۵��A��L�Ļ�������۵�ߣ���ԭ����?��
��9��A�ĵ�����L�ĵ�����B������������ˮ������Һ�����ȼ�յ�أ�д�����ֵ�صĸ����ĵ缫��Ӧʽ?��
��10��FԪ�ص������������MԪ�ص�����������ˮ���ﷴӦ�Ļ�ѧ����ʽ��?
?��
�ο��𰸣���1��? As ����2��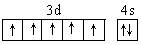 ��?��7?����3��?
��?��7?����3��? ?��
?��
��4�����ԣ� ?����5��? N O C?����6��?�������壻
?����5��? N O C?����6��?�������壻
��7��?�������ڵڢ���?��? Fe3����3d���Ϊ������ṹ�����ȶ�?��
��8�� NaH�����ӻ����H2O�ǹ��ۻ������9��H2��2e����2OH�D��2H2O?��
��10�� Al2O3��6HClO4��2Al(ClO4)3��3H2O ��9��10ÿ��2�֣�����ÿ��1�֣�
�����������
�����Ѷȣ�һ��
2��ѡ���� ����A��B����Ԫ�ص�ԭ�����������п������AB2�����ӻ��������
A��6��8? B��19��16? C��12��17? D��10��8
�ο��𰸣�C
���������A��Ԫ�ص�ԭ������Ϊ6��8�ķֱ��ǣ�CԪ�غ� OԪ�أ��γ�AB2�Ļ�����ΪCO2Ϊ���ۻ��������
B��Ԫ�ص�ԭ������Ϊ19��16�ķֱ��ǣ�KԪ�غ� SԪ�أ��γ�A2B�Ļ�����,����
C��Ԫ�ص�ԭ������Ϊ12��17�ķֱ��ǣ�MgԪ�غ� ClԪ�أ��γ�AB2�Ļ�����ΪMgCl2Ϊ���ӻ������ȷ��
D��Ԫ�ص�ԭ������Ϊ10��8�ķֱ��ǣ�NeԪ�غ� OԪ�أ������γɻ��������
�����Ѷȣ���
3��ѡ���� ����������Ȼͬλ��105B��115B����Ԫ�صĽ������ԭ������Ϊ10.80�����115B��ԭ�Ӱٷֱ��ǣ�?��
A .80��? B.20��? C. .40��? D������
�ο��𰸣�A
�������������M=M1*n1��+M2*n2��+����������115B��ԭ�Ӱٷֱ���x����105B�ٷֱ��ǣ�1-x�������ݹ�ʽ���Եõ�10*��1-x��+11x=10.80���õ�x=0.8����115B��ԭ�Ӱٷֱ���80����
�����Ѷȣ�һ��
4��ѡ���� X��Y��Z��Ϊ������Ԫ�ء���֪XԪ�ص�ij��ԭ�Ӻ��������ӣ�YԪ�ص�ԭ�Ӻ����������������������������2����ZԪ���ǵؿ��к�����ḻ��Ԫ�ء������к�������Ԫ�صĻ�ѧʽ��
��X2Y2Z2����X2YZ3����X2YZ2����X2Y2Z4����X3YZ4����XYZ3�����п��ܴ��ڵ��ǣ�?��
A����
B���ڢܢ�
C���ڢݢ�
D���٢ڢۢ�
�ο��𰸣�D
���������XԪ��ԭ�Ӻ��������ӣ�XΪH��Yԭ�Ӻ��������������Ǵ�����������2����YΪC��Z�ǵؿ��к�����ḻ��Ԫ�أ�ZΪO��������Ԫ�صĻ�����Ϊ��OHC��CHO����H2CO3����HCOOH����HOOC��COOH��
�����Ѷȣ�һ��
5��ѡ���� ����˵���д������
A��ԭ�Ӽ������ӵĺ�����Ӳ������ڸ�Ԫ�����ڵ���������
B��Ԫ�����ڱ��дӢ�B�嵽��B��10�����е�Ԫ�ض��ǽ���Ԫ�أ�
C���������ϡ������ԭ�ӵ���������������8��
D��ͬһԪ�صĸ���ͬλ�ص��������ʡ���ѧ���ʾ���ͬ
�ο��𰸣�AD
���������A����ȷ�����������ӵĺ�����Ӳ�����2�㣬�����ǵ�������Ԫ�ء���������ͬ����������ͬ��ͬһ��Ԫ�صIJ�ͬ���ػ���Ϊͬλ�أ����Ի�Ϊͬλ�ص�ԭ���������ʲ�ͬ����ѧ�������ƣ�D����ȷ����ѡAD��
�����Ѷȣ�һ��