1、选择题 含硒(Se)的保健品已开始进入市场。已知硒与氧、硫同主族,与溴同周期,则下列关于硒的叙述中,正确的是?(?)
A.非金属性比硫强
B.氢化物比HBr稳定
C.处于金属与非金属的分界线上
D.最高价氧化物的水化物为H2SeO4
2、填空题 五种短周期元素的部分性质数据如下:
元素
| T
| X
| Y
| Z
| W
|
原子半径(nm)
| 0.037
| 0.075
| 0.099
| 0.102
| 0.143
|
最高或最低化合价
| +1
| +5
-3
| +7
-1
| +6
-2
| +3
|
(1)Z离子的结构示意图为?。
(2)关于Y、Z两种元素,下列叙述正确的是?(填序号)。
a.简单离子的半径 Y > Z
b.气态氢化物的稳定性Y比 Z强
c.最高价氧化物对应水化物的酸性Z比Y强
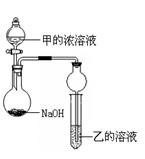
(3)甲是由T、X两种元素形成的10 e-分子,乙是由Y、W两种元素形成的化合物。
某同学设计了下图所示装置(夹持仪器省略)进行实验,将甲的浓溶液逐滴加入到NaOH固体中,烧瓶中即有甲放出,原因是?。一段时间后,观察到试管中的现象是?,发生反应的离子方程式是?。
(4)XO2是导致光化学烟雾的“罪魁祸首”之一。它被氢氧化钠溶液吸收的化学方程式是:2XO2 + 2NaOH =" M" + NaXO3 + H2O(已配平),产物M中元素X的化合价为?。
3、填空题 (5分)用“>”或“<”填空:
(1)第一电离能C ??N?(2)电负性Cl ??Br
(3)晶格能? KCl??CsCl?(4)硬度? MgO?CaO
(5)酸性? HClO3?HClO
4、计算题 将10.0 mL适量AlCl3溶液滴入10.0 mL 1.20 moL・L-1的NaOH溶液中,不断振荡,反应完全沉淀恰达最大值。问:?
(1)最多可得沉淀多少克??
(2)最后所得溶液中的溶质是什么?溶液浓度是多少?(假设体积具有加和性)
5、选择题 下列物质的性质按由弱到强或由低到高排列的? (? )
A.稳定性: PH3、H2S 、H2O、HF
B.酸性: H2CO3 、H2SO4、HClO4、HNO3
C.与氢气反应的难易程度:F2、Cl2、Br2 、I2
D.碱性: NaOH KOH RbOH CsOH