1、简答题 +2价金属元素M的原子中质子数比中子数少2个,2.1g的单质M与足量的盐酸反应共产生氢气0.05mol.试通过计算确定:
(1)该元素的摩尔质量为______g/mol,
(2)用
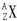
形式表示上题中金属元素M的原子______.
2、选择题 下列有关化学用语表达正确的是( )
A.Cl 的最外层电子排布式:
的最外层电子排布式: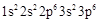
B.聚丙烯的结构简式: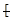 CH2-CH2-CH2
CH2-CH2-CH2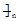
C.CH2Br2只能表示一种物质
D.NH3的电子式: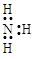
3、选择题 已知酸性强弱顺序为H2CO2>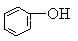 >HCO3―,下列化学方程式正确的是(?)
>HCO3―,下列化学方程式正确的是(?)
A. +H2O+CO2→
+H2O+CO2→ +Na2CO3
+Na2CO3
B. +H2O→
+H2O→ +NaOH
+NaOH
C. +Na2CO3→
+Na2CO3→ +NaHCO3
+NaHCO3
D. +NaHCO3→
+NaHCO3→ +H2CO3
+H2CO3
4、选择题 从元素化合价变化分析,下列变化中必须加入氧化剂才能发生的是(不考虑分解反应)
A.SO2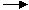 S
S
B. Na2SO3
Na2SO3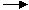 SO2
SO2
C.I ―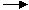 I2
I2
D.KClO3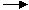 O2
O2
5、计算题 (8分)将32.64g铜与200mL一定浓度的硝酸反应,铜完全溶解产生的混合气体在标准状况下的体积为11.2L。请回答:
(1)NO的体积为 L,NO2的体积为 L(各保留二位有效数字)。
(2)待产生的气体全部释放后,向溶液加入VmL amol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为 mol/L。
(3)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3,至少需要30%的双氧水 g。