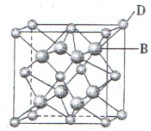
1、填空题 有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大的元素,C的2p轨道中有三个未成对电子,F原子核外电子数是B 与C核外电子数之和,D 是主族元素且与E同周期,E能形成红色或砖红色E2O和黑色的EO两种氧化物,D与B可形成离子化合物,其晶胞结构如图所示。请回答下列问题:
(1)E+离子基态时的电子排布式为_______________
(2)A2F的分子空间构型为_____________,FO3分子中F原子的杂化方式 ______________
(3)CA3极易溶于水,其原因主要是______________
(4)从图中可以看出,D 与B形成的离子化合物的化
学式为______________(用元素符号表示),该离子晶体的
密度为ag・cm-3,则晶胞的体积是____________(写出表达式即可,不用化简)
(5)已知E单质的晶体为面心立方最密堆积 (在晶胞的顶点和面心均含有一个E原子),则 E的晶体中E原子的配位数为?
2、选择题 某元素最高正价氧化物对应的水化物的化学式是H2XO4,这种元素的气态氢化物的化学式为
[? ]
A.HX
B.H2X
C.XH3
D.XH4
3、选择题 下列有关化学用语表示正确的是( )
A.乙炔的电子式:H:C:;C:H
B.对甲基苯酚的结构简式:

C.3,3-二甲基-1-戊烯的键线式:

D.乙醇分子的比例模型:

4、选择题 下列物质含有离子键的是( )
A.Cl2
B.NaOH
C.CO2
D.H2O
5、选择题 经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。下列判断正确的是
A.AlCl3为离子化合物
B.SiCl4为共价化合物
C.P 与Cl可形成离子键
D.K与Mg 形成共价键