1��ʵ���� ����(H2S)��һ�־��г�������ζ����ɫ���壬�о綾�������ڶ������������Լ���Ȼ���С�������ĺܶ�����������Ҳ������Ҫ���á�
���ϣ���H2S������ˮ?Լ1��2?����ˮ��ҺΪ��Ԫ���ᡣ
��H2S��������������ӷ�Ӧ���ɳ�����
��H2S�ڿ�����ȼ�գ�����ʵ���ɫ��
(1)ij��ѧС���������ȡH2S����֤�����ʵ�ʵ�飬����ͼ��ʾ��A����CuSO4��Һ��B�з���ʪ�����ɫʯ����ֽ��C����FeCl3��Һ��
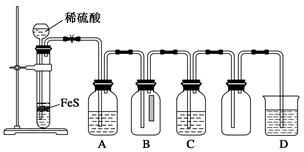
�ش��������⣺
��A���к�ɫ����(CuS)������A�з�����Ӧ�Ļ�ѧ����ʽΪ___________________��
��B�������__________________��
��C��ֻ��dz��ɫ��������������Һ��dz��ɫ����C�з�����Ӧ�����ӷ���ʽΪ______________��
��D��ʢ�ŵ��Լ�������________(����ĸ���)��
a��ˮ? b������
c��NaCl��Һ? d��NaOH��Һ
(2)Ϊ��һ��̽����2����Ļ������룫4����Ļ����ﷴӦ������С��ͬѧ�����������ʵ�顣
?
| ʵ�����
| ʵ������
|
ʵ��1
| ����Ũ�ȵ�Na2S��Na2SO3��Һ�������2��1���
| ����������
|
ʵ��2
| ��H2Sͨ��Na2SO3��Һ��
| δ�����Գ������ټ�������ϡ���ᣬ������������dz��ɫ����
|
ʵ��3
| ��SO2ͨ��Na2S��Һ��
| ��dz��ɫ��������
|
?
��֪������ƽ�ⳣ����
H2S��Kal��1.3��10��7��Ka2��7.1��10��15
H2SO3��Ka1��1.7��10��2��Ka2��5.6��10��8
�ٸ�������ʵ�飬���Եó����ۣ���__________�����£���4���������������2����Ļ����
�ڽ�SO2����ͨ��H2Sˮ��Һ��ֱ�����������б�ʾ��ҺpH��SO2��������仯��ϵʾ��ͼ��ȷ����________(����ĸ���)��
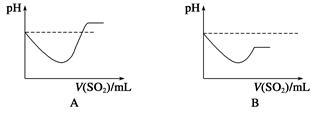
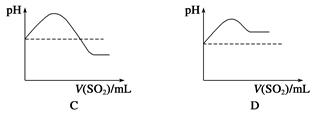
(3)�����أ�������H2S����Ag�����û���Ӧ����H2���ֽ�H2S����ͨ��װ�����۵IJ����ܣ�����Ƽ�ʵ�飬ͨ�����鷴Ӧ����֤��H2S��Ag�������û���Ӧ______��
�ο��𰸣�(1)��H2S��CuSO4=CuS����H2SO4����ɫʯ����ֽ���
��H2S��2Fe3��=S����2H����2Fe2��?��d
(2)������(�����Խ�ǿ)��C
(3)����Ӧ�������ͨ����������������Һ��(������ͭ��Һ���Ȼ�����Һ��)����ȥδ��Ӧ��H2S��ȼ�����۲쵽����ʵ���ɫ��˵����H2���ɣ��Ӷ�֤��H2S��Ag�������û���Ӧ(��������ʵ�飬���������𰸾���)
���������(1)����װ��ͼ��ʵ������Ϊ
FeS��H2SO4=FeSO4��H2S��
H2S��CuSO4=CuS����H2SO4
H2S H����HS���������ԣ���ʹ��ɫʯ����ֽ��졣
H����HS���������ԣ���ʹ��ɫʯ����ֽ��졣
2Fe3����H2S=S����2H����2Fe2��
Dװ������β��������Ӧѡ��NaOH��Һ��
(2)��SO32����S2���������������²��ܷ�����Ӧ����S��
��SO2��2H2S=3S����2H2O
SO2��H2O?H2SO3
H2SO3�����Դ���H2S������pH��С����(�ӽ�7)�ٵ�С����С��ԭ�������pHֵ��C����ȷ��
(3)H2S��2Ag=Ag2S��H2��Ӧ���ʵ����֤�Ƿ���H2���ɡ�
�����Ѷȣ�һ��
2������� ��6�֣�ֱ���ŷź�SO2���������γ����꣬Σ�������������Ƽ�ѭ�������ѳ������е�SO2.��
(1) ���Ƽ�ѭ�����У�Na2SO3��Һ��Ϊ����Һ������NaOH��Һ����SO2�Ƶã��÷�Ӧ�����ӷ���ʽ��?

�����ϱ��ж�NaHSO3��Һ��?�ԣ��û�ѧƽ��ԭ�����ͣ�������������������
�ڵ�����Һ������ʱ����Һ������Ũ�ȹ�ϵ��ȷ����(ѡ����ĸ):��������������������
a��c(Na��) = 2c(SO32��)��c(HSO3��)
b��c(Na��)>c(HSO3��)>c(SO32��)>c(H��) = c(OH��)
c��c(Na��)��c(H��)=c(SO32��)��c(HSO3��)��c(OH��)
�ο��𰸣���6�֣�(1) ?SO2��2OH��= SO32����H2O ?
��2����? HSO3-���ڣ�HSO3- SO32-+H+��HSO3-+H2O
SO32-+H+��HSO3-+H2O H2SO3+OH-��HSO3-�ĵ���̶�ǿ��ˮ��̶�? ab
H2SO3+OH-��HSO3-�ĵ���̶�ǿ��ˮ��̶�? ab
�����������1������������ǿ�SO2������������ܱ�����������Һ���գ���Ӧ�Ļ�ѧ����ʽ��SO2��2OH��= SO32����H2O��
��2������NaHSO3-Һ�д��ڣ�HSO3- SO32-+H+��HSO3-+H2O
SO32-+H+��HSO3-+H2O H2SO3+OH-�����ݱ��е����ݿ�֪����SO32����HSO3�������ʵ�����1�U1�������£���Һ�������Եģ���˵��HSO3���ĵ���̶ȴ���SO32����HSO3����ˮ��̶ȣ������Һ�������Եģ�����NaHSO3��Һ�����ԡ�
H2SO3+OH-�����ݱ��е����ݿ�֪����SO32����HSO3�������ʵ�����1�U1�������£���Һ�������Եģ���˵��HSO3���ĵ���̶ȴ���SO32����HSO3����ˮ��̶ȣ������Һ�������Եģ�����NaHSO3��Һ�����ԡ�
�ڸ��ݵ���غ��֪��c(Na��)��c(H��)=2c(SO32��)��c(HSO3��)��c(OH��)�����������Һ�����ԣ���c(H��) = c(OH��)��c(Na��) = 2c(SO32��)��c(HSO3��)��a��ȷ��c����ȷ�����ڲ�����ˮ��ǵ��룬��̶ȶ��Ǻ����ģ�����bҲ����ȷ�ģ���ѡab��
���������ж�����Ũ�ȴ�Сʱ��Ӧ�����úõ���ء������غ�������غ�Ȼ������ɡ�
�����Ѷȣ�һ��
3������� ��ȤС��̽��SO2���廹ԭFe3����I2������ʹ�õ�ҩƷ��װ����ͼ��ʾ��
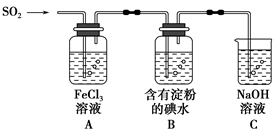
(1)SO2���廹ԭFe3���IJ�����________(�����ӷ���)���μӷ�Ӧ��SO2��Fe3�������ʵ���֮����________��
(2)����ʵ�鷽����������ʵ������ȡ����SO2����________��
A��Na2SO3��Һ��HNO3?B��Na2SO3������Ũ����
C���������ڴ�����ȼ��?D��ͭ����ŨH2SO4
(3)װ��C��������________________________________________________��
(4)��Ҫ��A��������Һ��ȡ���壬������е�ʵ��������裺��������ȴ�ᾧ�����ˡ���Ȼ�������һϵ�в�����û���õ���������________(�����)��
A����������? B��ʯ����? C��©��? D ���ձ�
E��������?F������
(5)������װ����ͨ�������SO2��Ϊ����֤A��SO2��Fe3��������������ԭ��Ӧ������ȡA�е���Һ���ֳ����ݣ������������ʵ�飺
�����٣�����һ����Һ�м�������KMnO4��Һ���Ϻ�ɫ��ȥ��
�����ڣ����ڶ�����Һ�м���KSCN��Һ������죬�ټ������Ƶ���ˮ����Һ��졣
�����ۣ�����������Һ�м�����ϡ�����ữ��BaCl2��������ɫ������
������������������________��ԭ����________________________________
(6)�ܱ���I����ԭ������SO2��������________________________________
�ο��𰸣�(1)Fe2����SO42����1��2��(2)BD��(3)���ն����SO2����ֹ��Ⱦ������(4)BF��(5)�����١�SO2Ҳ��ʹ����KMnO4��Һ��ɫ��(6)B����Һ��ɫ�䵭������ʧ
���������(1)SO2��2Fe3����2H2O=SO42����2Fe2����4H��
(2)ʵ������SO2��
Na2SO3��H2SO4(Ũ)=Na2SO4��SO2����H2O��Cu��2H2SO4(Ũ)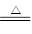 ?CuSO4��SO2����2H2O��HNO3������SO2���������ڴ�����ȼ�����ɵ�SO2�л���O2��
?CuSO4��SO2����2H2O��HNO3������SO2���������ڴ�����ȼ�����ɵ�SO2�л���O2��
(3)SO2�ж������ü�Һ���ա�
(4)�����õ�������Ϊ���������������ƾ��ơ�����̨�������õ�������Ϊ������̨��©�������������ձ���
�����Ѷȣ�һ��
4��ѡ���� ����ʵ����֤����SO2���ڵ���(? )
����ʹ����ʯ��ˮ�����?����ʹʪ�����ɫʯ����ֽ���?����ʹƷ����Һ��ɫ?��ͨ��������NaOH��Һ���ٵμ�BaCl2��Һ�а�ɫ�������ɣ��ó�������ϡ����?��ͨ����ˮ����ʹ��ˮ��ɫ���ٵμ�Ba(NO3)2��Һ�а�ɫ��������
A������֤��
B��ֻ�Т���֤��
C���ۢܢ���֤��
D��������֤��
�ο��𰸣�B
���������ֻ�Тݿ��ԣ�����������Ψһ�ģ�������ٵĻ���CO2������ڵ���HCl��HBr��HI�ȣ�����۵���Cl2,����ܵ���CO2��
�����Ѷȣ���
5������� ��17�֣�
��1��������SO2�������ᵼ����ˮ�к�������?���ѧʽ����Σ��ֲ��ͽ���������ŷŵ�SO2β���ñ���Na2SO3��Һ���տɵõ���Ҫ����ԭ��NaHSO3����Ӧ�Ļ�ѧ����ʽΪ?��
��2��SO2�ǿ������������ָ��֮һ������SO2��ԭKIO3����I2�ķ�Ӧ�ⶨ������SO2������ÿ����0.01mol I2���μӷ�Ӧ��SO2Ϊ������mol��

 ��3���ϳɰ��ķ�ӦN2(g)+3H2(g)
��3���ϳɰ��ķ�ӦN2(g)+3H2(g) 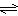 ?2NH3(g)? ��H = ��92.4 kJ��mol��1��һ�������µ��ܱ������У��÷�Ӧ�ﵽƽ�⣬Ҫ���N2��ת���ʣ����Բ�ȡ�Ĵ�ʩ��__________������ĸ���ţ���
?2NH3(g)? ��H = ��92.4 kJ��mol��1��һ�������µ��ܱ������У��÷�Ӧ�ﵽƽ�⣬Ҫ���N2��ת���ʣ����Բ�ȡ�Ĵ�ʩ��__________������ĸ���ţ���
a�������¶�?b���������? c������H2��Ũ��
d��������Դ:91������ 91eXAm.orgN2��Ũ��?e�������NH3 ?
 ��4����25���£���Ũ�Ⱦ�Ϊ0.1 mol��L-1��MgCL2��CuCl2�����Һ����μ��백ˮ��������__________�������ѧʽ�������ɸó��������ӷ���ʽΪ____________����֪25��ʱKsp[Mg(OH)2]=1.8��10-11,KsP[Cu(OH)2]=2.2��10-20��
��4����25���£���Ũ�Ⱦ�Ϊ0.1 mol��L-1��MgCL2��CuCl2�����Һ����μ��백ˮ��������__________�������ѧʽ�������ɸó��������ӷ���ʽΪ____________����֪25��ʱKsp[Mg(OH)2]=1.8��10-11,KsP[Cu(OH)2]=2.2��10-20��
 ��5����25���£���a mol��L-1�İ�ˮ��0.01 mol��L-1������������ϣ���Ӧ����Һ��c(NH4+)=c(Cl-)������Һ��_____________�ԣ���ᡱ������С����� ���ƶ�a ??0.01������ڡ����ڻ�С�ڣ���
��5����25���£���a mol��L-1�İ�ˮ��0.01 mol��L-1������������ϣ���Ӧ����Һ��c(NH4+)=c(Cl-)������Һ��_____________�ԣ���ᡱ������С����� ���ƶ�a ??0.01������ڡ����ڻ�С�ڣ���
�ο��𰸣���17�֣�
��1��H2SO4��H2SO3��2�֣���? SO2+Na2SO3+H2O��2NaHSO3��3�֣�
��2��0.05mol?��3�֣�?
��3��c e?��2�֣�
��4��Cu(OH)2 ��1�֣�?Cu2++2NH3��H2O=Cu(OH)2 ��+2NH4+��3�֣�
 ��5���У�1�֣������ڣ�2�֣���
��5���У�1�֣������ڣ�2�֣���
�����������
�����Ѷȣ�һ��