1、选择题 已知质量数为A的某阳离子Rn+,核外有X个电子,则核内中子数为
A.A-x
B.A-x-n
C.A-x+n
D.A+x-n
2、选择题 某溶液中可能含有OH-、CO32-、AlO2-、SiO32-、SO42-、Na+、Fe3+、Mg2+、Al3+等离子。当向该溶液中加入一定物质的量浓度的盐酸时,发现生成沉淀物质的量随盐酸的体积变化的如下图所示,下列说法正确的是

A.原溶液一定含有Na2SO4
B.反应最后形成的溶液中的溶质为NaCl
C.原溶液中一定含有的阴离子是OH-、CO32-、AlO2-、SiO32-
D.原溶液中含有CO32-与AlO2-的物质的量之比为1:1
3、填空题 短周期主族元素X、Y、Z、W、M、N 的原子序数依次增大,且原子最外层电子数之和为23。X 的原子半径比Y 的小,X 与W 同主族,Z 的最外层电子数是电子层数的3倍,M 是地壳中含量最高的金属元素。
(1)M的离子结构示意图____________,X、Y形成的含18电子的化合物的电子式____________
用电子式表示由W、Z形成的只含离子键的化合物的形成过程______________________
(2)Y、Z、M原子半径由大到小的顺序____________(用元素符号表示),Z的氢化物稳定性_____N的氢化物稳定性(填“>” “<”或 “=”)
(3)X和Z组成的化合物中,既含有极性共价键又含有非极性共价键的是_________(填化学式),此化合物可将碱性工业废水中的CN-氧化为碳酸盐和氨气,相应的离子方程式为:___________________________________________________________。
(4)由以上元素中两种或多种组成的化合物A、B、C、D有下列转化关系:
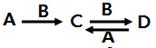
已知A溶液显碱性,可促进水的电离,用离子方程式表示A溶液显碱性的原因___________________,写出A与D反应的离子方程式______________________________。
4、选择题 应用元素周期,判断下列语句,其中正确的组合是()
①第一主族元素的氧化物都是离子化合物
②氢化物的稳定性:
③砷(As)的最高价氧化物对应水化物的酸性比磷酸弱
④第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性
⑤铊(Tl)与铝同主族,其单质既能与盐酸反应,又能与氢氧化钠溶液反应
⑥成(At)单质有颜色,且颜色较深
A.①③⑤
B.③⑥
C.②③④
D.④⑥
5、选择题 X、Y、Z、W是短周期元素,X为地壳中含量最高的金属元素;Y原子最外层电子数是电子总数的2/3;Z的最高正化合价与最低负化合价的代数和为4;W原子在短周期中原子半径最大。下列说法正确的是
A.ZO3和水反应形成的化合物是离子化合物
B.粘在试管内壁上的Z可以用YZ2洗涤
C.最高价氧化物对应水化物的碱性:X>W
D.X位于金属与非金属的分界线处,常用来做半导体材料