1、实验题 把温度为13℃、浓度为1.0 mol/L的酸溶液和1.1 mol/L的碱溶液各50 mL混合[溶液密度均为1 g/mL,所生成溶液的比热容c=4.184 J/(g・℃)],轻轻搅动。测得酸碱混合液的温度变化数据如下
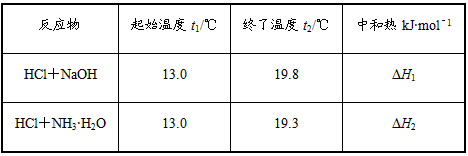
(1)试计算上述两组实验测出的中和热: ΔH1=__________;ΔH2=____________。
(2)实验中碱液过量的目的是____________________________。
(3)两组实验结果有差异的原因是____________________________。
2、选择题 已知OCN-中每种元素都满足8电子稳定结构,在反应OCN-+OH-+Cl2→CO2+N2+Cl-+H2O(未配平)中,如果有6 mol Cl2完全反应,则被氧化的OCN-的物质的量是
A.2 mol
B.3 mol
C.4 mol
D.6 mol
3、选择题 已知:HCN(aq)与NaOH(aq)反应的△H=-12.1 kJ・mol-1;HCl(aq)与NaOH(aq)反应的△H=-55.6 kJ・mol-1。则HCN在水溶液中电离的△H等于
[? ]
A. -67.7 kJ・mol-1
B. -13.5 kJ・mol-1
C. +43.5 kJ・mol-1
D. +67.7 kJ・mol-1
4、选择题 使18 g焦炭发生不完全燃烧,所得气体中CO占1/3体积,CO2占2/3体积,已知:C(s) +1/2O2(g)=CO(g)
△H=- Q1 kJ/mol;CO(g)+1/2O2(g)=CO2(g) △H = -Q2kJ/mol。与这些焦炭完全燃烧相比较,损失的热量是
[? ]
A.1/3 Q1kJ
B.1/3 Q2 kJ
C.1/3(Q1+Q2) kJ
D.1/2 Q2 kJ
5、选择题 在298K、1.01×105Pa下,将22g CO2通入1mol・L-1 NaOH溶液750mL中充分反应,测得反应放出x kJ的热量。已知该条件下,1mol CO2通入2mol・L-1 NaOH溶液1L中充分反应放出y kJ的热量。则CO2与NaOH溶液反应生成NaHCO3的热化学方程式正确的是
[? ]
A.CO2(g)+NaOH(aq)=NaHCO3(aq) △H=-(2y-x)kJ・mol-1
B.CO2(g)+NaOH(aq)=NaHCO3(aq) △H=-(2x-y)kJ・mol-1
C.CO2(g)+NaOH(aq)=NaHCO3(aq) △H=-(4x-y)kJ・mol-1
D.2CO2(g)+2NaOH(aq)=2NaHCO3(aq) △H=-(8x-2y)kJ・mol-1