1、简答题 四种短周期元素的微粒信息如下表:
| 元素代号 | Q | R | X | Z
微粒信息
离子: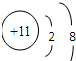
单质分子:R2
离子:X3+
一种原子:Z
|
已知Q、R、X在同一周期,R2常温常压下为气体
完成下列填空:
(1)Q位于周期表第______周期第______族.化合物Q2Z的电子式为______(用元素符号表示).
(2)Q、R、X的原子半径由大到小的顺序为______(用元素符号表示);Q、R、X、Z中金属性最强的是______(用元素符号表示).
(3)Q与X两者的最高价氧化物对应的水化物之间发生反应的离子方程式为:______.
2、选择题 同周期的X、Y、Z三种元素,已知其最高价氧化物对应的水化物的酸性强弱顺序是:HXO4>H2YO4>H3ZO4,则下列各判断中不正确的是( )
A.原子序数:X>Y>Z
B.单质的氧化性:X>Y>Z
C.气态氢化物的稳定性:X>Y>Z
D.它们形成的阴离子X-、Y2-、Z3-的电子层结构相同,且离子半径大小:X->Y2->Z3-
3、推断题 四种短周期元素A、B、C、D原子序数依次增大。A、B、C三种元素原子核外电子层数之和是5。A、B两种元素原子最外层电子数之和等于C元素原子最外电子层上的电子数;B元素原子最外电子层上的电子数是它电子层数的2倍,A和C可以形成化合物CA3,B与D的原子序数之比为3∶4。请回答:
(1)化合物CA3的化学式是_____________________________。
(2)写出A和C化合生成CA3反应的平衡常数表达式__________________________。在一定条件下要使该反应平衡向右移动,可采取的措施有___________。
A.缩小反应容器容积 B.增大反应容器容积 C.使用合适的催化剂 D.及时分离出生成物
(3)由四种元素中的三种元素组成的物质甲属于盐类,其水溶液呈酸性,请用离子方程式表示其呈酸性的原因_______________________________,若用pH试纸测定0.1 mol/L的甲溶液的pH,实验操作是_________________________________。
(4)乙和丙为含有上述四种元素的常见无机盐,二者均既可与盐酸又可与烧碱溶液反应。则乙和丙的化学式为乙:________________;丙_____________________。
(5)写出乙溶液与硫酸氢钠溶液反应的离子方程式________________________________。
4、推断题 A、B、C、D、E、F、G均是原子序数小于36的元素。A的基态原子外围电子排布式为3s2;B原子的L电子层的P能级上有一个空轨道;?C元素的基态原子最外层有3个未成对电子,次外层有2个电子;?D?的原子的2p轨道上有1个电子的自旋方向与其它电子的自旋方向相反;E是海水中除氢、氧元素外含量最多的元素;F和G在周期表中既处于同一周期又位于同一族,且原子序数F比G小2。
根据信息回答下列问题:?
(1)C的外围电子排布图为___________?。C与氢元素可分别形成含10个电子的分子、阴离子和阳离子,阳离子中中心原子的杂化类型为__________;分子的VSEPR模型名称为___________;阴离子的立体构型为______________。
(2)G的价电子排布式为___________。用电子式表示化合物AE2的形成过程________。
(3)F与BD易形成配合物F(BD)5,在F(BD)5中F的化合价为_______;与BD分子互为等电子体的分子和离子分别为____________和____________(填化学式)。
(4)E有多种含氧酸根①EO-?②EO2-?③EO3-?④EO4-,其中空间构型为四面体型的是__________。(填序号)
(5)B、C、D、E原子相互化合形成的分子有多种,请列举两种分子内所有原子都满足最外层8电子稳定结构的分子:______________________(写分子式)?
5、选择题 下列叙述正确的是
[? ]
A.只有非金属元素能形成含氧酸盐
B.所有主族元素的原子,形成单原子离子时化合价和它的族序数数值相等
C.同一元素的各种同位素的性质相同
D.M层电子数为奇数的所有主族元素所在的族的序数与该元素原子的M层电子数数值相等