1、填空题 (8分)已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数分别为:
醋酸? Ka= 1.75×10-5
碳酸? Ka1= 4.30×10-7? Ka2 = 5.61×10-11
亚硫酸? Ka1= 1.54×10-2? Ka2 = 1.02×10-7
(1)写出碳酸的第一步电离平衡常数表达式:Ka1 = ??;
碳酸的第一步电离比第二步电离?(填“容易” 或 “困难”)。
(2)在相同条件下,试比较H2CO3、HCO3-和HSO3-的酸性强弱:??>?>?
(3)若保持温度不变,在醋酸溶液中加入少量盐酸,下列量会变小的是?(填序号)
A.c(CH3COO-)
B.c(H+)
C.醋酸的电离平衡常数
D.醋酸的电离度
2、选择题 常温下,将少量水加入下列物质中,相关量变化正确的是( )
A.AgCl悬浊液中?c(Cl-)变小
B.0.1mol/LCH3COOH溶液中?c(H+)变小
C.0.1mol/LNa2CO3?c(HCO3-)变大
D.0.1mol/LNH4Cl溶液中?n(OH-)变小
3、选择题 下列事实能说明亚硝酸是弱电解质的是
[? ]
①亚硝酸钠溶液的PH大于7 ②用HNO2溶液做导电试验,灯泡很暗
③HNO2溶液不与Na2SO4溶液反应 ④0.1mol・L-1HNO2溶液的PH=2.1
A.①②③
B.②③④
C.①④
D.①②④
4、选择题 氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是
[? ]
A.再通入少量氯气,c(H+)/c(ClO-)减小
B.通入少量SO2,溶液漂白性增强
C.加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-)
D.加入少量水,水的电离平衡向正反应方向移动
5、选择题 下列过程表达式中,属于电离方程式的是
A.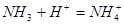
B.
C.
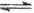
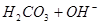
D.