| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ֪ʶ���ȫ����Ӧ������ƽ����йؼ��㡷��Ƶ����̣�2017�����°棩(��)
��4��CH4��H2O�ڴ������淢����ӦCH4+H2O  CO+3H2��T��ʱ����1 L�ܱ�������Ͷ��1 mol CH4��1 mol H2O��g����5Сʱ���÷�Ӧ��ϵ�ﵽƽ��״̬����ʱCH4��ת����Ϊ50% ��������¶��µ�ƽ�ⳣ��??���������С�������λ���֣��� CO+3H2��T��ʱ����1 L�ܱ�������Ͷ��1 mol CH4��1 mol H2O��g����5Сʱ���÷�Ӧ��ϵ�ﵽƽ��״̬����ʱCH4��ת����Ϊ50% ��������¶��µ�ƽ�ⳣ��??���������С�������λ���֣�����5���Լ״�Ϊȼ�ϵ����͵�أ���ɱ�����������Ϊȼ�ϵĴ�ͳȼ�ϵ�أ�Ŀǰ�õ��㷺���о�����ͼ��Ŀǰ�о��϶��һ�����������ȼ�ϵ�ع���ԭ��ʾ��ͼ���ش��������⣺  ��B���ĵ缫��ӦʽΪ?�� �����ø�ȼ�ϵ������Դ����ʯī���缫�������ͭ��Һ������·��ת��1mole-ʱ��ʵ�������ĵļ״��������������ϴ���ԭ����?�� ��6��25��ʱ������Ƶ�Ksp=4.0��10-8,̼��Ƶ�Ksp=2.5��10-9����20ml̼��Ƶı�����Һ����μ���8.0��10-4 mol��L-1�IJ������Һ20ml���ܷ��������??����ܡ����� 3������� N2O5��һ�������������������ʺ��Ʊ��ܵ����ǵĹ�ע��һ���¶��£��ں����ܱ�������N2O5�ɷ������з�Ӧ�� 2N2O5(g) �P 4NO2(g) + O2(g).��H��0
(3)��T2�¶��£���Ӧ1000 sʱ���NO2��Ũ��Ϊ4.98mol��L-1����T2 __________ T1��(����ڡ������ڡ���С�ڡ�) 4������� (1)��ѧƽ�ⳣ��K��ʾ���淴Ӧ�Ľ��г̶ȣ�KֵԽ��ʾ__________?�� 5������� CO2��Ŀǰ�����к�����ߵ�һ���������壬���ƺ�����CO2�ǽ������ЧӦ����Ч;����
���¶�һ��ʱ�������̼��[�����]��CO2��ת����?���������С�� �����䡱���� �ڸ÷�Ӧ������ӦΪ?��������š����ȷ�Ӧ�� ��3���������£���3 molH2��1molCO2�����������ڹ̶��ݻ�Ϊ2L���ܱ������У��������·�Ӧ��3H2��g��+CO2��g�� 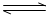 CH3OH��g��+H2O��g����2minĩ�÷�Ӧ�ﵽƽ�⣬���CH30H��Ũ��Ϊ0��2mol��L�������жϲ���ȷ����___?_�� CH3OH��g��+H2O��g����2minĩ�÷�Ӧ�ﵽƽ�⣬���CH30H��Ũ��Ϊ0��2mol��L�������жϲ���ȷ����___?_��a���������´˷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪ 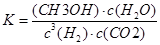 b��H2��ƽ����Ӧ����Ϊ0��3mol����L��s�� c��CO2��ת����Ϊ60% d�������������ܶȲ��ٸı�ʱ���÷�Ӧһ���ﵽƽ��״̬ ��4����ͼ���Ҵ�ȼ�ϵ�أ��������ҺΪKOH��Һ���Ľṹʾ��ͼ����a��ͨ�����?����Ҵ���������������b���缫�Ϸ����ĵ缫��Ӧ�ǣ�?�� 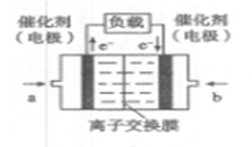 ��5��CO2����Ȼ��ѭ��ʱ����CaCO3��Ӧ��CaCO3��һ���������ʣ��� 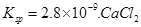 ��Һ��Na2CO3��Һ��Ͽ��γ�CaCO3�������ֽ��������CaCl2��Һ��Na2CO3��Һ��ϣ���Na2CO3��Һ��Ũ��Ϊ ��Һ��Na2CO3��Һ��Ͽ��γ�CaCO3�������ֽ��������CaCl2��Һ��Na2CO3��Һ��ϣ���Na2CO3��Һ��Ũ��Ϊ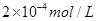 �������ɳ�������CaCl2��Һ����СŨ��Ϊ?�� �������ɳ�������CaCl2��Һ����СŨ��Ϊ?�� |
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ�����л�ѧ֪ʶ�㽲�⡶�������Һ.. | |
| �����Ŀ |