1、填空题 A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸.
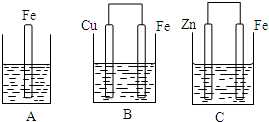
(1)B中正极的电极反应式为______.
(2)C中被腐蚀的金属是______,负极的电极反应式为______.
(3)A、B、C中铁被腐蚀的速率,由快到慢的顺序是______.
参考答案:(1)B中铁做负极,铜做正极,电解质溶液为硫酸,则正极反应为2H++2e-=H2↑,故答案为:2H++2e-=H2↑;
(2)C形成原电池,锌比铁活泼,做原电池的负极而被氧化,负极反应为Zn-2e-=Zn2+,
故答案为:Zn,Zn-2e-=Zn2+;
(3)A发生化学腐蚀,B发生电化学腐蚀,C锌比铁活泼,铁做原电池的正极而被保护,电化学腐蚀的速率大于化学腐蚀的速率,故答案为:B>A>C.
本题解析:
本题难度:一般
2、填空题 (8分)现有如下两个反应:
(A)NaOH + HCl="===" NaCl + H2O?(B)Zn + CuSO4 = ZnSO4 + Cu
(1)根据两反应本质, 判断能设计成原电池的是?。
(2)根据你的选择完成下列问题:
正极材料:?;负极材料:?
电解质:?。
正极反应式为:?
负极反应式为:?
参考答案:(1)? B? 1 分?(2) Cu? 1分? Zn? 1分? CuSO4?1分
Cu2+?+2e- ="==" Cu? Zn-2e-===Zn2+?各2分
本题解析:(1)在原电池中,有电子的移动,说明只有氧化还原反应才能设计成原电池。A是中和反应,不是氧化还原反应,不能设计成原电池。B是氧化还原反应,可以设计成原电池。
(2)根据总反应式可知,锌是还原剂,失去电子。硫酸铜是氧化剂,得到电子,所以锌是负极,正极的金属性必须弱于锌的。由于铜离子在正极得到电子,所以电解质溶液是硫酸铜。
本题难度:一般
3、选择题 某同学利用家中废旧材料制作一个可使玩具扬
声器发出声音的电池,装置如右图所示。下列
说法正确的是?(?)
A.电流方向为:
铝质易拉罐→导线→扬声器→导线→炭棒
B.铝质易拉罐将逐渐被腐蚀
C.电池总反应为:4Al+3O2+6H2O=4Al(OH)2
D.炭棒上发生的主要反应为:2H++2e-=H2↑
参考答案:BC
本题解析:略
本题难度:一般
4、填空题 北京时间2013年12月2日凌晨1时30分,我国的“嫦娥三号”月球探测器在西昌卫星发射中心发射升空,发射“嫦娥三号”月球探测器的火箭推进器中装有还原剂肼(N2H4)和氧化剂N2O4,当它们混合时,即产生大量的氮气和水蒸气,并放出大量的热。已知0.4 mol气态肼和足量N2O4气体反应生成氮气和水蒸气时放出219.3 kJ的热量。
(1)写出肼和N2O4反应的热化学方程式: ;
(2)已知H2O(l)=H2O(g) ΔH=+44 kJ・mol-1,则16 g气态肼与足量N2O4气体反应生成氮气和液态水时,放出的热量是 ;
(3)肼除应用于火箭燃料外,还可作为燃料电池的燃料,由肼和空气构成的碱性燃料电池的负极反应式为: ,正极反应式为: ;
(4)向次氯酸钠溶液中通入一定物质的量的氨气可生成肼,写出反应的离子方程式: 。
参考答案:(1)2N2H4(g)+N2O4(g) = 3N2(g)+4H2O(g) ΔH=-1096.5kJ・mol-1(热化学方程式和反应热各1分)
(2)318.1 kJ(未写单位不得分)
(3)N2H4-4e-+4OH- = N2+4H2O O2+4e-+2H2O = 4OH-
(4)2NH3+ClO-= N2H4+Cl-+H2O
本题解析:(1)已知0.4 mol气态肼和足量N2O4气体反应生成氮气和水蒸气时放出219.3 kJ的热量。则2mol液态肼放出的热量为219.3 kJ×5=1096.5 kJ
所以反应的热化学方程式为:2N2H4(g)+N2O4(g) = 3N2(g)+4H2O(g) ΔH=-1096.5kJ・mol-1
(2)已知H2O(l)=H2O(g) ΔH=+44 kJ・mol-1
所以有反应的热化学方程式为:2N2H4(g)+N2O4(g) = 3N2(g)+4H2O(l) ΔH=-1272.5kJ・mol-1
16 g气态肼的物质的量="16g/32g/mol=0.5mol," 放出的热量Q=1272.5 kJ /4="318.1" kJ
(3)由肼和空气构成的碱性燃料电池的负极反应式为:N2H4-4e-+4OH- = N2+4H2O 正极反应式为:O2+4e-+2H2O = 4OH-
(4)向次氯酸钠溶液中通入一定物质的量的氨气可生成肼, 次氯酸钠是氧化剂,被还原为氯化钠,氨气做还原剂,被氧化为肼。2NH3+ClO-= N2H4+Cl-+H2O
考点:热化学方程式的书写,电极反应式的书写。
本题难度:一般
5、填空题 在由铜片、锌片和200 mL稀硫酸组成的原电池中,若锌片口只发生电化学腐蚀,当在铜片上共放出2.24 L气体(标准状况)时,稀H2SO4刚好用去一半,则产生这些气体消耗锌___________g,共有___________mol电子通过导线,原H2SO4溶液的浓度是________mol/L
参考答案:6.5,0.20,1.0
本题解析:有关的电极反应为:负极Zn-2e-====Zn2+正极2H++2e-====H2↑n(H2)=0.10mol,则转移的电子为0.20mol,则n(Zn)=0.10mol,m(Zn)=6.5g。
c(H2SO4)=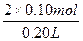 =1mol/L。
=1mol/L。
本题难度:简单