1、选择题 从化学原理和经济利益角度分析,下列从海水中提取镁单质的方法最可行的是
A.海水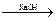
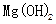
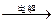

B.海水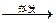
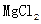
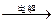

C.海水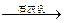
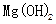
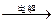

D.海水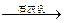
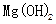
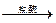
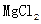
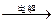

参考答案:D
本题解析:略
本题难度:简单
2、填空题 下图是某工厂对海水资源进行综合利用的示意图。

请回答下列问题:
(1)请列举一种海水淡化的方法 。?
(2)工业上常用离子交换膜电解槽生产NaOH,电解过程中大量通过离子交换膜的离子是 ,NaOH在电解槽的 室生成,由饱和食盐水制取NaOH的化学方程式为 。?
(3)侯氏制碱法中向饱和食盐水中通入CO2和NH3制得NaHCO3,先通入 (填化学式),理由是 。再由NaHCO3制得纯碱,化学方程式为 。?
(4)镁是一种用途很广泛的金属材料,目前世界上60%的镁从海水中提取。已知有关物质的熔沸点数据如下:
?
| MgO
| MgCl2
|
熔点/℃
| 2 852
| 714
|
沸点/℃
| 3 600
| 1 412
|
?
结合表中数据和实际生产情况说明,工业上生产镁采用电解MgCl2而不是电解MgO的理由 。?
参考答案:(1)蒸馏法(或电渗析法、冷冻法、离子交换法等)
(2)Na+ 阴极 2NaCl+2H2O 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑
(3)NH3 NH3极易溶于水,有利于充分吸收CO2,增大溶液中碳酸氢根的浓度 2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
(4)MgO比MgCl2熔点高,电解MgO比电解MgCl2耗能多
本题解析:(2)离子交换膜电解饱和食盐水,只有Na+通过离子交换膜,阴极H+得电子生成氢气,阴极区溶液中OH-浓度增大
本题难度:一般
3、选择题 下列冶炼方法中,不能将化合物中的金属元素还原为金属单质的是( )。
A.加热Al2O3
B.加热HgO
C.电解熔融NaCl
D.铝粉和Fe2O3共热
参考答案:A
本题解析:金属钠是活泼金属,用电解法制取,汞用加热HgO制取,A项中加热Al2O3难以分解;D项中铝粉和Fe2O3组成铝热剂,可将Fe2O3中的铁还原成单质。
本题难度:一般
4、选择题 下列说法不正确的是( )
A.玻璃工业不涉及氧化还原反应
B.在潮湿的中性环境中,金属的电化学腐蚀主要是吸氧腐
C.一般合金的硬度比各成分金属要大,多数合金的熔点也比成分金属要低
D.有氧气参加的任何发光、发热的剧烈的化学反应才能称之为燃烧
参考答案:D
本题解析:
本题难度:一般
5、填空题 (12分)综合利用海水可以制备食盐、纯碱、金属镁、溴等物质,其流程如下图所示:
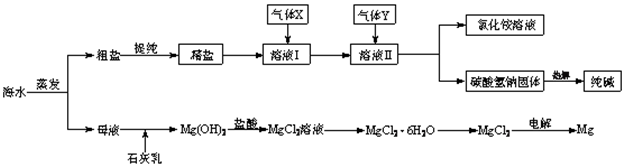
(1)粗盐中含有硫酸钠、氯化镁、氯化钙等可溶性杂质,为除去这些杂质而得精盐,进行如下操作:①溶解;②加过量的BaCl2溶液;③加过量的NaOH溶液;④加过量的Na2CO3溶液;⑤ ;⑥加适量的盐酸;⑦ 。
(2)溶液Ⅱ中发生反应的化学方程式是: 。
(3)Mg(OH)2沉淀中因混有Ca(OH)2,可选用___ ___ 溶液进行洗涤以除之。
(4)高温灼烧六水合氯化镁晶体(MgCl2・6H2O)所得固体是氧化镁,试写出该反应的化学方程式________ __ 。
(5)若在母液中通入氯气可提取海水中的溴,反应的离子方程式为:_____?_______。
参考答案:(1)过滤?蒸发结晶(只写“蒸发”给分,只写“结晶”不给分)
(2)NaCl + NH3 + CO2 + H2O=NaHCO3 + NH4Cl(2分,不追究沉淀符号)
(3)MgCl2或写“氯化镁”
(4)MgCl2・6H2O MgO+ 2HCl↑+5H2O↑?(5)Cl2 + 2Br―=2Cl―+ Br2
MgO+ 2HCl↑+5H2O↑?(5)Cl2 + 2Br―=2Cl―+ Br2
本题解析:(1)考查粗盐的提纯加入碳酸钠溶液之后,溶液中含有硫酸钡、氢氧化镁和碳酸钡以及碳酸钙沉淀,需要通过过滤除去。酸化后通过蒸发结晶即得到氯化钠。
(2)根据生成物碳酸氢钠和氯化铵可知,反应的方程式为NaCl + NH3 + CO2 + H2O=NaHCO3 + NH4Cl,
(3)由于氢氧化镁的溶解度小于氢氧化钙的,所以要除去氢氧化镁中的氢氧化钙,可以加入氯化镁生成氢氧化镁和氯化钙而除去。
(4)氯化镁在溶液中存在水解平衡,水解是吸热的,所以直接加热得不到氯化镁,而是得到氧化镁,方程式为MgCl2・6H2O MgO+ 2HCl↑+5H2O↑。
MgO+ 2HCl↑+5H2O↑。
(5)氯元素的非金属性强于溴元素的,所以氯气能把溴离子氧化生成溴单质,方程式为Cl2 + 2Br―=2Cl―+ Br2。
本题难度:一般