1、选择题 “便携式乙醇测量仪”以燃料电池为工作原理,在酸性环境中乙醇被氧化为X,其中一个电极的反应式为:CH3CH2OH-2e- =?X + 2H+。下列说法中正确的是
A.电池内部H+由正极向负极移动
B.另一极的电极反应式为:O2 + 4e- + 2H2O = 4OH-
C.乙醇在正极发生反应,电子经过外电路流向负极
D.电池总反应为:2CH3CH2OH+O2→2CH3CHO+2H2O
参考答案:D
本题解析:A.电池内部H+由正极向正极移动,错误;B.由于是酸性电解质溶液,另一极的电极反应式为:O2 + 4e- +? 4H+= ?2H2O,错误;C.乙醇在负极发生反应,电子经过外电路流向正极,错误;D正确;
本题难度:一般
2、填空题 (14分)砷(As)广泛分布于自然界,其原子结构示意图是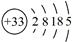 。
。
(1)砷位于元素周期表中 族,其气态氢化物的稳定性比NH3 (填“强”或“弱”)。
(2)砷的常见氧化物有As2O3和As2O5,其中As2O5热稳定性差。根据下图写出As2O5分解为As2O3的热化学方程式: 。
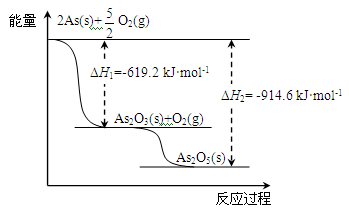
(3)砷酸盐可发生如下反应:AsO43-+2I
参考答案:
本题解析:
本题难度:困难
3、选择题 A、B、C三种金属片,把A、B?用导线连接后同时浸入稀硫酸溶液中,A是负极;把B、C?用导线连接后同时浸入稀硫酸溶液中,C发生还原反应.三种金属的活动性顺序是( )
A.A>B>C
B.C>B>A
C.A>C>B
D.B>A>C
参考答案:原电池中较活泼金属作负极,较不活泼金属作正极;负极上失电子发生氧化反应,正极上得电子发生还原反应.
把A、B?用导线连接后同时浸入稀硫酸溶液中,A是负极,B是正极,所以金属的活泼性A>B;
把B、C?用导线连接后同时浸入稀硫酸溶液中,C发生还原反应,B发生氧化反应,所以金属的活泼性B>C,
所以这三种金属的活泼性大小顺序为A>B>C.
故选A.
本题解析:
本题难度:简单
4、选择题 有A、B、C、D四种金属。将A与B用导线连接起来浸入电解质溶液中,B不易腐蚀。将A、D分别投入等浓度盐酸溶液中,D比A反应剧烈。将铜浸入B的盐溶液中,无明显变化。如果把铜浸入C的盐溶液中,有金属C析出。据此判断它们的活动性由强到弱的顺序是
[? ]
A.D>C>A>B
B.D>A>B>C
C.D>B>A>C
D.B>A>D>C
参考答案:B
本题解析:
本题难度:一般
5、选择题 镍氢电池的总反应式是?H2+2NiO(OH)?
2Ni(OH)2,根据此反应式判断,此电池放电时,负极上发生反应的物质是( )
A.NiO(OH)
B.Ni(OH)2
C.H2
D.H2和NiO(OH)
参考答案:C
本题解析:
本题难度:简单