1、填空题 (10分)铅蓄电池是常用的化学电源,其电极材料分别是Pb和PbO2,电解液为稀硫酸。放电时,该电池总反应式为:Pb+PbO2+2H2SO4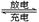 2PbSO4+2H2O。请根据上述情况判断:
2PbSO4+2H2O。请根据上述情况判断:
(1)该蓄电池的负极材料是_________,放电时发生_________(填“氧化”或“还原”)反应。
(2)该蓄电池放电时,电解质溶液的酸性_________(填“增大”、“减小”或“不变”),电解质溶液中阴离子移向_________(填“正”或“负”)极。
(3)已知硫酸铅为不溶于水的白色沉淀,生成时附着在电极上。试写出该电池放电时,正极的电极反应_______________________________________(用离子方程式表示)。
(4)氢氧燃料电池具有启动快、效率高等优点,其能量密度高于铅蓄电池。若电解质为KOH溶液,则氢氧燃料电池的负极反应式为__________________________________。该电池工作时,外电路每流过1×103 mol e-,消耗标况下氧气_________m3。
参考答案:本题共10分
(1)Pb(1分); 氧化(1分)
(2)减小(1分); 负(1分)
(3)PbO2+2 e-+SO2-4+4H+=PbSO4+2H2O(2分)
(4)H2-2e-+2OH-=2H2O(2分); 5.6(2分)
本题解析:(1)该蓄电池的负极发生氧化反应,根据总化学反应方程式可知,Pb作负极,放电时发生氧化反应;
(2)放电时消耗硫酸,生成硫酸铅和水,所以电解质溶液的酸性减小,放电相当于是原电池,所以电解质溶液中的阴离子移向负极;
(3)放电时的正极即是PbO2发生还原反应,得电子与硫酸结合生成硫酸铅,电极反应式为
PbO2+2 e-+SO2-4+4H+=PbSO4+2H2O;
(4)氢氧燃料电池中的电解质溶液若为KOH溶液,则在负极发生氧化反应的氢气,失去电子,与氢氧根离子结合生成水,电极反应式为H2-2e-+2OH-=2H2O,该电池工作时,正极的反应式为O2+4e-+2H2O=4OH-,所以外电路每流过1×103 mol e-,则消耗氧气得物质的量是1000/4=250mol,标准状况下的体积是250mol×22.4L/mol=5600L,合5.6m3。
考点:考查电化学反应原理的应用,电极反应式的书写,氧化还原反应的计算
本题难度:一般
2、选择题 近年,科学家们发明了一种能够给电子设备提供动力的生物燃料电池.该电池包括两个涂覆着酶的电极,它们处于充满空气和少量氢气的玻璃槽中.由于气体可以混合从而省去了昂贵的燃料隔离膜,其工作原理如图所示.下列说法正确的是
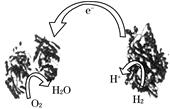
A.左边为该电池的负极
B.该电池可在高温环境下使用
C.该电池负极反应为:H2-2e-=2H+
D.该电池正极反应为O2+4e-=2O2-
参考答案:C
本题解析:由电池示意图可知,H2→H+,是H2被氧化的过程,通入H2的一极为原电池的负极,发生反应:H2-2e-=2H+;O2→H2O,是O2被还原的过程,通入O2的一极为原电池的正极,发生反应:O2+4e-+4H+=2H2O,以此解答该题。
A.左边通入O2,发生还原反应,为电池的正极,故A错误;
B.该电池包括两个涂覆着酶的电极,高温下会使酶变性,不能在高温下使用,故B错误;
C.通入H2的一极为原电池的负极,发生反应:H2-2e-=2H+,故C正确;
D.通入O2的一极为原电池的正极,发生反应:O2+4e-+4H+=2H2O,故D错误,答案选C。
点评:该题以新型化学电源为载体,重点考查学生对原电池原理,特别是电极名称和电极反应式书写的了解掌握情况,意在培养学生的逻辑推理能力。答题时注意把握题给信息,为解答该题的关键,做题时注意审题,能根据生成物判断电极反应并书写电极方程式。
本题难度:一般
3、选择题 理论上不能设计原电池的化学反应是
[? ]
A.CH4 + 2O2 → CO2 + 2H2O
B.HNO3 + NaOH = NaNO3 + H2O
C.2H2 + O2 = 2H2O
D.2FeCl3 + Fe = 3FeCl2
参考答案:B
本题解析:
本题难度:简单
4、选择题 化学电池可以直接将化学能转化为电能,化学电池的本质是
A.化合价的升降
B.电子的转移
C.氧化还原反应
D.电能的储存
参考答案:C
本题解析:化学电池的本质是氧化还原反应,通过氧化还原反应实现了电子的转移,从而将化学能转变为电能。答案选C。
点评:本题非常简单基础。
本题难度:简单
5、填空题 全钒液流电池是一种活性物质呈循环流动液态的电池,目前钒电池技术已经趋近成熟。如图是钒电池基本工作原理示意图:

请回答下列问题:
(1)硫酸在电池技术和实验室中具有广泛的应用,在传统的铜锌原电池中,硫酸是 ,实验室中配制硫酸亚铁时需要加入少量硫酸,硫酸的作用是 。
(2)钒电池是以溶解于一定浓度硫酸溶液中的不同价态的钒离子(V2+、V3+、VO2+、V)为正极和负极电极反应的活性物质,电池总反应为VO2++V3++H2O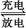 +V+2H+。放电时的正极反应式为 ,充电时的阴极反应式为 。放电过程中,电解液的pH (选填“升高”“降低”或“不变”)。
+V+2H+。放电时的正极反应式为 ,充电时的阴极反应式为 。放电过程中,电解液的pH (选填“升高”“降低”或“不变”)。
(3)钒电池基本工作原理示意图中“正极电解液”可能是 。
a.V、VO2+混合液
b.V3+、V2+混合液
c.V溶液
d.VO2+溶液
e.V3+溶液
f.V2+溶液
(4)能够通过钒电池基本工作原理示意图中“隔膜”的离子是 。
参考答案: (1)电解质溶液 抑制硫酸亚铁的水解
(2)V+2H++e- VO2++H2O V3++e-
VO2++H2O V3++e- V2+ 升高
V2+ 升高
(3)acd (4)H+
本题解析: (1)传统的铜锌原电池中,锌与酸反应生成氢气,故硫酸为电解质溶液;硫酸亚铁容易水解,且水解显酸性,加入少量硫酸,可以抑制其水解变质。(2)正极反应是还原反应,由电池总反应可知放电时的正极反应为V+2H++e- VO2++H2O;充电时,阴极反应为还原反应,故为V3+得电子生成V2+的反应。(3)充电时阳极反应式为VO2++H2O-e-
VO2++H2O;充电时,阴极反应为还原反应,故为V3+得电子生成V2+的反应。(3)充电时阳极反应式为VO2++H2O-e- V+2H+,故充电完毕的正极电解液为V溶液,而放电完毕的正极电解液为VO2+溶液,故正极电解液可能是选项acd。(4)充电和放电过程中,正极电解液与负极电解液不能混合,起平衡电荷作用的是加入的酸,故H+可以通过隔膜。
V+2H+,故充电完毕的正极电解液为V溶液,而放电完毕的正极电解液为VO2+溶液,故正极电解液可能是选项acd。(4)充电和放电过程中,正极电解液与负极电解液不能混合,起平衡电荷作用的是加入的酸,故H+可以通过隔膜。
考点:燃料电池
本题难度:一般