1、选择题 在一定温度下的密闭容器中,加入1 mol CO和1 mol H2O,发生反应:CO(g)+H2O(g)  CO2(g)+H2(g),达到平衡时测得n(H2)为0.5 mol,下列说法不正确的是( )
CO2(g)+H2(g),达到平衡时测得n(H2)为0.5 mol,下列说法不正确的是( )
A.在该温度下平衡常数K=1
B.平衡常数与反应温度无关
C.CO的转化率为50%
D.其他条件不变改变压强平衡不移动
参考答案:B
本题解析:反应CO(g)+H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)
起始物质的量? 1? 1? 0? 0
变化物质的量? 0.5? 0.5? 0.5? 0.5
平衡物质的量? 0.5? 0.5? 0.5? 0.5
A正确;B错,平衡常数受温度影响;C正确;D正确;
本题难度:一般
2、选择题 在300℃时,改变起始反应物中n(H2)对反应N2(g) + 3H2(g)  2NH3(g)+Q(Q>0)的影响如右图所示。下列说法正确的是
2NH3(g)+Q(Q>0)的影响如右图所示。下列说法正确的是
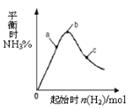
A.反应在b点达到平衡
B.b点H2的转化率最高
C.c点N2的转化率最高
D.a、b、c三点的平衡常数Kb > Ka > Kc
参考答案:C
本题解析:增大氢气的浓度,平衡向正反应方向移动,但氢气的转化率是降低的,氮气的转化率是提高的,所以图像中氮气转化率最高的应该是氢气的量最大时的点为C点。由于温度不变故平衡常数是相同的。
本题难度:一般
3、选择题 在密闭容器中发生反应a X(气)+b Y(气) c W(气)+d Z(气),若反应达到平衡后,保持温度不变,将气体压缩到原来的1/2体积,再次达到平衡时,Z的浓度是原平衡的1.8倍,下列叙述中正确的是
c W(气)+d Z(气),若反应达到平衡后,保持温度不变,将气体压缩到原来的1/2体积,再次达到平衡时,Z的浓度是原平衡的1.8倍,下列叙述中正确的是
A.平衡向逆反应方向移动
B.a+b>c+d
C.W的体积分数增大
D.X的转化率降低
参考答案:AD
本题解析:略
本题难度:简单
4、选择题 对于m A (g)+n B (g) p C(g)+q D(g)的平衡体系,当升高温度时,平衡混合气体对氢气的相对密度从16.5变成16.9,则下列说法正确的是? (? )
p C(g)+q D(g)的平衡体系,当升高温度时,平衡混合气体对氢气的相对密度从16.5变成16.9,则下列说法正确的是? (? )
A.m+n> p+q,正反应是放热反应
B.m+n> p+q,正反应是吸热反应
C.m+n< p+q,逆反应是放热反应
D.m+n< p+q,逆反应是吸热反应
参考答案:BD
本题解析:升高温度,平衡向吸热反应方向移动。而当升高温度时,平衡混合气体对氢气的相对密度从16.5变成16.9,密度增大,说明气体的体积减小,故吸热反应方向与气体的体积减小的方向是一个方向,所以,当m+n> p+q,正反应是吸热反应;当m+n< p+q,逆反应是吸热反应。
本题难度:一般
5、选择题 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示,下列表述正确的是( )。

A.化学方程式为:2M N
N
B.t2时,正逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
参考答案:D
本题解析:由图象可知N为反应物,M为生成物,然后找出在相同时间段内变化的M、N的物质的量之比(与是否达平衡无关)以确定M、N在化学方程式中的化学计量数之比,即该反应的化学方程式是:2N M。t2时刻M、N的物质的量相等,但此时M、N的物质的量仍在发生变化,反应未达到平衡状态,因此正反应速率不等于逆反应速度。t3时刻及t3时刻之后,M、N的物质的量不再改变,证明已达平衡状态,此时正、逆反应速率相等。
M。t2时刻M、N的物质的量相等,但此时M、N的物质的量仍在发生变化,反应未达到平衡状态,因此正反应速率不等于逆反应速度。t3时刻及t3时刻之后,M、N的物质的量不再改变,证明已达平衡状态,此时正、逆反应速率相等。
本题难度:一般