1、简答题 (14分)I.已知:C(s)+H2O(g) CO(g)+H2(g)?ΔH
CO(g)+H2(g)?ΔH
一定温度下,在1.0 L密闭容器中放入1 mol C(s)、1 mol H2O(g)进行反应,反应时间(t)与容器内气体总压强(p)的数据见下表:
时间t/h
| 0
| 1
| 2
| 4
| 8
| 16
| 20
| 25
| 30
|
总压强p/100 kPa
| 4.56
| 5.14
| 5.87
| 6.30
| 7.24
| 8.16
| 8.18
| 8.20
| 8.20
|
回答下列问题:
(1)下列哪些选项可以说明该可逆反应已达平衡状态?。
A.混合气体的密度不再发生改变? B.消耗1 mol H2O(g)的同时生成1 mol H2
C.ΔH不变? D.v正(CO) = v逆(H2)
(2)由总压强P和起始压强P0表示反应体系的总物质的量n总,n总=____ mol;由表中数据计算反应达平衡时,反应物H2O(g)的转化率α =_____(精确到小数点后第二位)。
Ⅱ.硫单质及其化合物在工农业生产中有着重要的应用。
(1)已知25℃时:xSO2 (g)+2xCO(g)=2xCO2 (g)+Sx (s)? ΔH=ax kJ/mol?①
2xCOS(g)+xSO2 (g)=2xCO2 (g)+3Sx (s)? ΔH=bx kJ/mol。?②
则反应COS(g)生成CO(g)、Sx (s)的热化学方程式是?。
(2)向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸至过量。其中H2S、HS?、S2?的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与滴加盐酸体积的关系如图所示(忽略滴加过程H2S气体的逸出)。试分析:
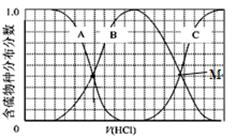
①B曲线代表?分数变化(用微粒符号表示);滴加过程中,溶液中一定成立:
c(Na+)=?。
②M点,溶液中主要涉及的离子方程式?。
参考答案:(14分,每空2分))
I.(1)AD?(2)P/P0? 79.82%(或0.80)
II.(1)xCOS(g) =" xCO(g)+" Sx(s)?ΔH=0.5(bx-ax)kJ/mol
(2)①HS- ?c(Na+)=3[c(H2S)+c(HS-)+c(S2-)](由物料守恒得出)
或c(Na+)= c(Cl-)+c(OH-)+c(HS-)+2c(S2-)-c(H+)(由电荷守恒得出)
②M:2S2-+3H+=HS-+H2S
本题解析:I.(1)因为该反应中有固体参与,所以气体的质量一直变化,而容器的体积不变,所以当混合气体的密度不再发生改变时,证明已达平衡状态,正确;B、消耗1 mol H2O(g)的同时生成1 mol H2
都是正反应方向,不能证明反应达平衡状态,错误;C、反应方程式固定,则反应的ΔH固定,所以不能判断化学平衡状态是否到达,错误;D、CO和H2的物质的量之比是1:1,所以v正(CO) = v逆(H2)时符合正逆反应速率相等,说明反应达平衡状态,正确,答案选AD;
(2)开始时气体的物质的量为1mol,根据恒温恒容条件下,气体的物质的量之比等于气体的压强之比得n总=P/P0mol,由表中数据可知平衡时的压强为8.20(100Kpa),开始的压强为4.56(100Kpa),设消耗水蒸气的物质的量为xmol,则平衡时H2O(g)、CO(g)、H2(g)的物质的量(mol)分别为1-x、x、x,根据n总=P/P0mol,得1-x+x+x=8.20/4.56,解得x=0.7982,所以反应物H2O(g)的转化率α =79.82%;
II.(1)根据盖斯定律得目标方程式=(②-①)/2,所以所求热化学方程式为xCOS(g) =" xCO(g)+" Sx(s)?ΔH=0.5(bx-ax)kJ/mol;
(2)①向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸至过量,盐酸先与氢氧化钠反应生成氯化钠和水,再与硫化钠反应生成硫氢化钠,此时溶液中S2?的含量逐渐减小,HS?的含量逐渐增大,继续滴加盐酸,则HS?与氢离子结合生成硫化氢,则溶液中H2S的含量逐渐增大,HS?的含量逐渐减小,所以A、B、C分别代表S2? 、HS?、H2S的分数变化。B曲线代表、HS?的分数变化;根据物料守恒,Na元素的浓度是S元素浓度的3倍,可得滴加过程中,溶液中一定成立的是c(Na+)=3[c(H2S)+c(HS-)+c(S2-)];滴加的过程中溶液中始终存在Na+、Cl-、HS-、S2-、OH-、H+,根据电荷守恒可得c(Na+)= c(Cl-)+c(OH-)+c(HS-)+2c(S2-)-c(H+);
②M点表示HS-与S2-分数相等,所以溶液中发生的总的离子方程式为2S2-+3H+=HS-+H2S
本题难度:一般
2、选择题 化学平衡主要研究下列哪一类反应的规律? (? )
A.可逆反应? B.任何反应 C部分反应? D.气体反应
参考答案:A
本题解析:化学平衡主要研究可逆反应,答案选A。
点评:该题是常识性知识的考查,难度不大,侧重对学生基础知识的巩固与效率,学生记住即可。
本题难度:简单
3、选择题 甲、乙、丙三个密闭容器中分别充入一定量的A和B,发生反应: 。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别如下图表所示:
。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别如下图表所示:

下列说法正确的是
A.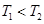 ,且该反应为吸热反应
,且该反应为吸热反应
B.x=2
C.若平衡后保持温度不变,改变容器体积平衡不移动
D.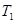 ℃下,若起始时向甲容器中充入0.5molA、1.5molB,平衡时A的转化率为25%
℃下,若起始时向甲容器中充入0.5molA、1.5molB,平衡时A的转化率为25%
参考答案:C
本题解析:A.对于甲、乙来说,起始投入量相同,而反应乙首先达到平衡说明温度T2>T1。在平衡时C(C)(乙) <C(C)(甲),说明升高温度,化学平衡向逆反应方向移动。根据平衡移动原理:升高温度,化学平衡向吸热方向移动,逆反应方向是吸热反应,所以正反应是放热反应。错误。B.对乙、丙来说,反应的温度相同,而起始投入量丙是乙的2倍。在其它条件不变的情况下,若增加反应物的浓度,化学平衡不发生移动,则达到化学平衡时C(C)的浓度也应该是乙的2倍。现在2C(C)(乙)=C(C)(丙).说明改变反应物的浓度,化学平衡没有发生改变。只有在反应前后气体体积相等的可逆反应中,改变压强或改变浓度,化学平衡不移动。所以1+X=2,X=1.错误。C. 若平衡后保持温度不变,由于该反应是反应前后气体体积相等的可逆反应。改变容器体积,即改变压强,根据平衡移动原理,化学平衡不移动。正确。D.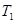 ℃下,起始时向甲容器中充入1.5molA、0.5molB,达到化学平衡时A的转化率为:(0.75÷1.5)×100%=50%.在该温度下,若起始时向甲容器中充入0.5molA、0.5molB,平衡时A的转化率为25%,然后再加入1molB,,增大反应物的浓度,平衡向正反应方向移动,故A的转化率就大于25%。错误。
℃下,起始时向甲容器中充入1.5molA、0.5molB,达到化学平衡时A的转化率为:(0.75÷1.5)×100%=50%.在该温度下,若起始时向甲容器中充入0.5molA、0.5molB,平衡时A的转化率为25%,然后再加入1molB,,增大反应物的浓度,平衡向正反应方向移动,故A的转化率就大于25%。错误。
本题难度:一般
4、选择题 下列事实不能用勒夏特列原理解释的是
A.开启啤酒瓶后,瓶中马上泛起大量泡沫
B.光照氯水,颜色变浅
C.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的转化率
D.由H2、I2(g)、HI组成的平衡体系,加压后颜色加深
参考答案:D
本题解析:由H2、I2(g)、HI组成的平衡体系,加压后体积变小引起的颜色加深,D错误。
本题难度:简单
5、选择题 将1 mol SO2和1mol O2通入一容积不变的密闭容器中,在一定温度和催化剂作用下,发生反应:2SO2(g)+O2(g) 2SO3(g)。反应达到平衡时SO3为0.3 mol。若此时移走0.5 mol O2和0.5 mol SO2,则重新达到平衡后,SO3的物质的量
2SO3(g)。反应达到平衡时SO3为0.3 mol。若此时移走0.5 mol O2和0.5 mol SO2,则重新达到平衡后,SO3的物质的量
A.等于0.3 mol
B.等于0.15 mol
C.小于0.15 mol
D.大于0.15 mol,小于0.3 mol
参考答案:C
本题解析:移走0.5 mol O2和0.5 mol SO2相当于对容器进行减压一半操作,因此平衡逆向移动,所以SO3的物质的量小于0.15 mol。答案选C。
点评:改变影响移动的一个条件,平衡向减弱这种改变的方向移动。
本题难度:一般