| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ֪ʶ���ܽᡶ����ľ���������������ռ�����Ƶ������ѵ��2017����ϰ�棩(��)
��2������ҺC���CuSO4��5H2O����Ҫ��������Ũ����?�����������˵Ȳ��������ձ���©���⣬���˲��������õ���һ�����������������ڴ˲����е���Ҫ������������������ ��3���Ʊ�CaCO3ʱ��������Ӧ�Ļ�ѧ����ʽ��?������������������������������?����ʵ��������а����ݳ�����ѡ������װ���е�?����?������ţ�װ�����հ����� ���ձ��е�Һ�嶼Ϊˮ�� 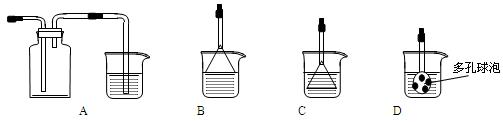 ��4�����ⶨ��ҺA��Fe2+��Ũ�ȣ�������100 mL 0.1 mol�MLKMnO4����Һ�����Ƹ���Һʱ�����ձ�������������ͷ�ι��⣬�����һ�ֲ���������?����������?�������ò��������м�����ˮ���ӽ��̶���1��2cmʱ��Ӧ�������������������μ�����ˮ����Һ�İ�Һ��������̶�����ƽ�� �ο��𰸣���ÿ��2�֣���16�֣� ����������� �����Ѷȣ�һ�� 3������� ˮ�ܿ��г�SiO2�⣬����9.24% CoO��2.78% Fe2O3��0.96% MgO��0.084 % CaO��������ȡ�ܵ���Ҫ�����������£� �ο��𰸣���16�֣���1��12��2�֣���90��2�֣� �����������1����ͼ��֪�������¶ȣ��ܵĽ��������������60��ʱ����Ч��̫�ͣ�90��ʱ������Ч����120��ʱ������Ч�������ԣ�����120��ʱ�����ɱ�ԶԶ����90��ʱ�����ɱ��������ѽ����¶�Ϊ90�棬����ѽ���ʱ��Ϊ12h����2���۲��֪���÷�Ӧ���漰������ԭ��Ӧ����������1����ƽ����Na2Fe6(SO4)4(OH)12��ϵ��Ϊ1��������ԭ���غ�ɵ�Fe2(SO4)3��ϵ��Ϊ3��������ԭ���غ�ɵ�Na2SO4��ϵ��Ϊ5��������ԭ���غ�ɵ�Na2CO3��ϵ��Ϊ6������̼ԭ���غ�ɵ�CO2��ϵ��Ϊ6��������ԭ���غ�ɵ�H2O��ϵ��Ϊ6����3Fe2(SO4)3+6H2O+6Na2CO3=Na2Fe6 (SO4)4(OH)12��+5Na2SO4+6CO2������3��c(Ca2+)/c(Mg2+)=[c(Ca2+)?c2(F��)]/[c(Mg2+)?c2(F��)]= Ksp��CaF2��/ Ksp��MgF2��=(1.11��10��10)/( 7.40��10��11)=1.5����4�����������������������Կ������ε��룬�����������Գ�������֮ǰ�����ķ�Ӧ��������ϡ�������ʱ�������������ӣ�����̼���Ƴ���ʱ����������ӣ���������Ƴ�ȥ�ơ�þʱ����ķ����ӣ��������麟���������ʱ�����笠����ӣ���ȥ��ˮ�ϲ����ܳ����л��еĿ��������ʣ�����ϴ�ӡ�����Ȳ�������5���ŵ�ʱ����ܷ�ӦΪCoO2+LiC6=LiCoO2+C6����Ԫ����+4��Ϊ+3�ۣ��Ԫ���ɺϽ��е�0��Ϊ+1�ۣ�����ӦʽΪLi��e��=Li+��������������������������������������������ϵķ�Ӧ������������ӦʽΪCoO2+ e��+ Li+= LiCoO2�� �����Ѷȣ�һ�� 4��ʵ���� �����������ޣ�����һ��һС��֧�Թܺ�ϡ���ᣬ�ס�����ͬѧ��������������Ƥ�� �ο��𰸣���1���� ��2����ʹ��Ӧ���Թܿ������ռ��Թܵĵײ���Ȼ�����������ƶ� ��3������Ƥ��������ʳ�ȡ� ����������ü�ͬѧ��Ƶ�װ��ʵ��ʱ�����������������ܶ�С���������ڴ��Թܶ�������ʱ����Ѵ��Թܻ������ƻ�С�Թ����������ƶ����Ϳɰѿ������Թ������ų����Ӷ��ռ�����Ϊ������һ�Թ����������������ͬѧ��Ƶ�װ��ʵ�飬���������������Թܵķ�϶�ų���ͬʱ����С�Թ��еĿ��������ų����������ռ��������������� �����Ѷȣ��� 5��ѡ���� ��ͼ��һ��ʵ�����Ʊ������װ�ã����ڷ���������ռ��������ж����塣���и�����������������װ�ý���ʵ����� �ο��𰸣�CD ����������� �����Ѷȣ�һ�� |
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ���߿���ѧ�ؿ�֪ʶ�㡶��ѧ������.. | |
| �����Ŀ |