1������� ����ͼ��ʾװ�ý���ʵ�飬���ش��������⣺
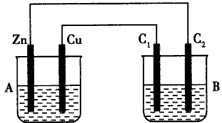

��1���ж�װ�õ����ƣ�A��Ϊ__________________��B��Ϊ________________________��
��2������Ϊ_________�����缫��ӦʽΪ________________________��ͭ��Ϊ________�����缫��ӦʽΪ________________________ ��ʯī��C1Ϊ_______�����缫��ӦʽΪ____________________________��ʯī��C2����������ʵ������Ϊ________����Ӧ������B����Һ��pHֵ________��(����С�����䣬������������ˮ)
��3����C2������224 mL���壨��״���£�����������________�����ӻ���٣�__________g
�ο��𰸣���1��ԭ���(1��)?����(1��)
��2��������1�֣� Fe-2e-=Fe2+?��2�֣�
������1�֣�Cu2++2e-="Cu" ��2�֣�
������1�֣� 2Cl--2e-=Cl2����2�֣�?���������ɣ���Һ��죨2�֣� ����1�֣�
��3������? 0.56����1�֣�
�����������1��A�ؿɷ����Է���������ԭ��Ӧ��Ϊԭ��ء�B��Ϊ���ء���2��A��������ͭ���ã�����������Fe-2e-=Fe2+?ͭ��������Cu2++2e-=Cu����B����ʯī��C1���Դ������������������2Cl--2e-=Cl2��ʯī��C2��������2H2O -2e-=H2 + 2OH-?��3��C2����H2224mL,���ʵ���Ϊ0.01mol��ת��0.02mol���ӣ�Ӧ��Ӧ0.01mol��������Ϊ0.56g.
�����Ѷȣ�һ��
2������� ij�����ŷŵĹ�ҵ��ˮ�к�Fe3+��Al3+��Cu2+������Ϊ�˼��ٻ�����Ⱦ�����Ϊ�������÷���м��������ѧ�Լ�������ͼ�������õ������졢Al2O3�ͽ���Cu���ش��������⣺
��1������A�ijɷ���______�����û�ѧʽ��ʾ��
��2��д��B��D�����ӷ���ʽ______���÷�Ӧ����������______��2molCl2�μӷ�Ӧת�Ƶ�����______mol����ҺD�еμ�KSCN��Һ��������______��
��3����ҺE��ɫ��Ӧ�ʻ�ɫ���Լ�H��______���û�ѧʽ��ʾ����D��E��Ӧ�����ӷ���ʽ��______��
��4���ֱ�д��������������ڹ�ҵ�ϵ�һ����Ҫ��;������______��������______��
�ο��𰸣���1����������ͼ�п���֪������ɻ������졢Al2O3�ͽ���Cu���ȼӹ������ۣ�2Fe3++Fe�T3 Fe2+�����ڽ����˳���������ͭ��ǰ�棬�������۰�ͭ�û�������Cu2++Fe=Fe2++Cu�����˵õ�Fe��Cu��
�ʴ�Ϊ��Fe��Cu��
��2������������ҺB�к���Al3+��Fe2+������ˮ��+2�۵������ӱ���ˮ������2Fe2++Cl2=2Fe3++2Cl-���÷�Ӧ����������Ԫ�ش�0�۱�Ϊ�����е������ӣ����ϼ۽�������������1mol�����μӷ�Ӧ�õ�2mol���ӣ���2mol�����μӷ�Ӧ�õ�4mol���ӣ���ҺD�к���Fe3+����KSCN��ҺFe3++3SCN-?Fe��SCN��3��Һ���ɫ��
�ʴ�Ϊ��2Fe2++Cl2=2Fe3++2Cl-��Cl2��4����Һ���ɫ��
��3������Al3+��Fe2+�����ǿ����������ȿ��Ժ�ǿ�ᷴӦ�����Ժ�ǿ�Ӧ����������������� ҺE��ɫ��Ӧ�ʻ�ɫ˵�����������ӣ�˵���Լ�H���������ƣ��Ӽ��ȷ�����ӦAl3++3OH-=Al��OH��3����ǿ�����Al��OH��3+OH-=AlO2-+2H2O���ܷ�ӦΪ��Al3++4OH-=AlO2-+2H2O��
�ʴ�Ϊ��NaOH��Al3++4OH-=AlO2-+2H2O��
��4������Ϊ������������ɫ��ĩ�����������ᡢ��ī���ȹ�ҵ�У�Ҳ��������������������ͨ�����õ������ʣ����Կ�������ԭ�ϣ��������۵�ߣ��������ͻ���ϣ�Ҳ������ҵ�����ȣ�
�ʴ�Ϊ����ɫ�����Ϳ�ϵȣ��ͻ���ϣ�
���������
�����Ѷȣ�һ��
3������� ��ͼ��ʾˮ�����Թ�����һö���������������۲죺
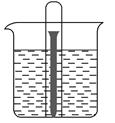
(1)�����������⣬�������ĸ�ʴ����________��ʴ��
(2)���Թ���Һ����������ԭ��Һ��________�ԣ�����________��ʴ���缫��ӦʽΪ��������____________________��������____________________��
(3)���Թ���Һ���½�����ԭ��Һ��________�ԣ�����________��ʴ���缫��ӦʽΪ��������____________________��������____________________��
�ο��𰸣�(1)�绯ѧ��(2)�����Ի��С�����
2Fe��4e��=2Fe2����O2��2H2O��4e��=4OH��
(3)��ǿ���ᡡ���⡡Fe��2e��=Fe2����2H����2e��=H2��
�������������ԭ��صĹ��������������ֲ�ͬ�IJ���(FeΪ������̼Ϊ����)���е������Һ���γɱպϻ�·����֪�����ĸ�ʴ���ڵ绯ѧ��ʴ�����ݽ�����ʴ������ԭ���������֪���Թ���Һ��������˵�����Թ���ѹǿ��С���Թ������屻�������£�������������ʴ�Ľ�����ݴ�д���缫��Ӧʽ���Թ���Һ���½���˵�����Թ�������ѹǿ����Թ��ڲ��������������£����������ⸯʴ�Ľ�����ݴ�д���缫��Ӧʽ��
�����Ѷȣ�һ��
4������� ��8�֣���ͼ��ʾװ���У��ס��ҡ��������ձ����ηֱ�ʢ��NaOH��Һ��CuSO4��Һ��K2SO4��Һ���缫��Ϊʯī�缫��
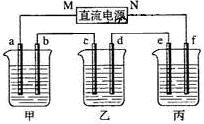
��ͨ��Դ������һ��ʱ��������c�缫����������16g���ݴ˻ش��������⣺
��1���缫b�Ϸ����ĵ缫��ӦΪ?��
��2������缫e�����ɵ������ڱ�״̬�µ������?��
��3���������Һ��pH?�����������С�����䡱����������ԭ��?��
��4�������������ͭȫ����������ʱ����ܷ�������У�Ϊʲô��
?��
�ο��𰸣�
��1��4OH����4e��=2H2O + O2����2�֣�
��2��5.6 L ��2�֣�
��3������1�֣���Ϊ�൱�ڵ��ˮ��1�֣�
��4���ܣ���ΪCuSO4��Һ��ת��ΪH2SO4��Һ����Ӧ��Ϊ���ˮ�ķ�Ӧ��2�֣�
�����������1������c�缫�������ӣ���c�������ķ�ӦΪ��Cu2++2e��=Cu����c��Ϊ�������ɴ˿��Ƴ�bΪ������aΪ������MΪ������NΪ����������ΪNaOH���൱�ڵ��H2O������b��Ϊ������OH���ŵ磬��4OH����4e��=2H2O + O2����
(2)��������16gCu����ʱ��ת�Ƶĵ���Ϊ0.5mol����������·�Ǵ����ģ���ÿ���ձ��еĵ缫��ת�Ƶ���������ȵġ�����ΪK2SO4���൱�ڵ��ˮ���ɷ���ʽ2H2O 2H2��+O2����֪������2molH2��ת��4mol���ӣ����Ե�������Ӧ��ת��0.5mol����ʱ�����ɵ�H2Ϊ0.25mol������µ����Ϊ0.25mol��22.4L/mol=5.6L��
2H2��+O2����֪������2molH2��ת��4mol���ӣ����Ե�������Ӧ��ת��0.5mol����ʱ�����ɵ�H2Ϊ0.25mol������µ����Ϊ0.25mol��22.4L/mol=5.6L��
(3)�����൱�ڵ��ˮ����NaOH��Ũ������pH���
(4)ͭȫ����������ʱ�ΪH2SO4�����Ե�ⷴӦ���ܽ��С�
�����Ѷȣ�һ��
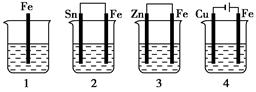
5��ѡ���� ����ͼ��ʾ����������ʢ�к�ˮ���������б���ʴʱ���ɿ쵽����˳����(����)
A��4��2��1��3
B��2��1��3��4
C��4��2��3��1
D��3��2��4��1
�ο��𰸣�A
�����������1���ο���2�й�����ԭ��أ��������Fe>Sn,����Fe��ԭ��صĸ�����Fe��Ӧ��ʴ�����ʱ�1�죻3�й�����ԭ��أ����ڽ������Zn>Fe,����Fe��ԭ��ص����������ȱ�����������Zn,����Fe����ʴ�ķ�Ӧ���ʱ�1����4�ǵ��أ�Fe���Դ���������ӣ��������������ķ�Ӧ��Fe-2e-=Fe2+��Fe��ʴ�����ʱ�2�졣����������б���ʴʱ���ɿ쵽����˳����4��2��1��3��ѡ��ΪA.��
�����Ѷȣ�һ��