1、选择题 关于二氧化硫和二氧化氮叙述正确的是
A.两种气体都是无色有毒的气体,且都可用水吸收以消除对空气的污染
B.二氧化硫与过量的二氧化氮混合后通入水中能得到两种常用的强酸
C.两种气体都具有强氧化性,因此都能够使品红溶液褪色
D.两种气体溶于水都可以与水反应,且只生成相应的酸
2、选择题 常温下,由下列实验事实得出结论错误的是
A.SO2使品红溶液和溴水褪色,说明SO2具有漂白性
B.BaSO4不溶于水和酸,在医学上可用作钡餐
C.洒落在地上的汞可在其表面撒硫磺除去
D.蔗糖加入浓硫酸后变黑,说明浓硫酸具有脱水性
3、选择题 基于实验现象的推论,你认为合理的是(?)
选项
| 实验现象
| 推论
|
A
| 乙烯气体可以使溴水褪色
| 乙烯发生取代反应
|
B
| 浓硫酸电导率比较低
| 硫酸浓度大时是弱电解质
|
C
| 氨气用于喷泉实验
| 氨气极易溶于水
|
D
| 硝酸溶液使pH试纸先变红后变白
| 硝酸酸性太强不能用pH试纸检测
4、选择题 下列物质加入溴水,经振荡,不因发生化学反应而使溴水褪色的是
[? ]
A.Na2S
B.NaOH
C.甲苯
D.裂化汽油
5、实验题 为探究铜与浓硫酸的反应,甲、乙两同学分别设计了图1、图2所示装置,将足量铜和10 mL 18 mol・L-1浓硫酸共热,直到无气体生成为止(假定反应前后试管中溶液的体积不变)。
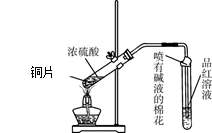 ? ?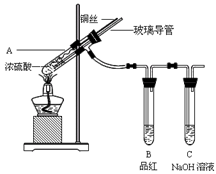
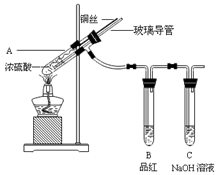 图1?图2 图1?图2
(1)比较两实验装置,图2装置的优点是:①?;②?。
(2)①甲根据所学的化学知识认为还有一定量的硫酸剩余。甲认为硫酸剩余的理论依据是?。
②下列药品中能够用来证明反应结束后的烧瓶中确有硫酸剩余的是_______。(选填编号)
A.过量铁粉
B.氯化钡溶液
C.银粉
D.碳酸氢钠溶液
|
(3)乙在拆除图2装置前,不打开胶塞,为使装置中的残留气体完全被吸收,应当采取的操作是?。
(4)为定量测定当剩余硫酸浓度不大于何值时,铜与硫酸就不能反应,甲、乙两位同学进 行了如下设计:
①甲方案:将产生的气体缓缓通过预先称量过的盛有?的干燥管,反应结束后再次称量,干燥管质量增加m g。其余酸浓度为?mol・L-1。
②乙方案:分离出反应后的溶液并加蒸馏水稀释至1 000 mL,取20.00 mL于锥形瓶中,滴入2~3滴?,(选填“酚酞”、“甲基橙”)用0.1000mol・L-1标准NaOH溶液进行滴定(已知氢氧化铜开始沉淀的pH约为5),用去NaOH溶液V mL。其余酸浓度为?mol・L-1。
③甲、乙两方案比较,你认为误差较大的是?,理由是?。