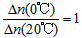1、填空题 化肥是农业生产最基础而且是最重要的物质投入.工业上利用N2和H2合成氨,其化学方程式为:N2(g)+3H2(g)?2NH3(g)△H<0
(1)下表为不同温度下该反应的平衡常数.由此可推知,表中T1______573K(填“>”、“<”或“=”).
| T/K | T1 | 573 | T2
K
1.00×107
2.45×105
1.88×103
|
(2)将一定量的N2和H2的混合气放入某密闭容器中发生上述反应.
①下列措施中可提高氢气的转化率的有______(填字母).
A.升高温度?B.使用催化剂
C.增大压强?D.循环利用和不断补充氮气
②在一定温度和压强下,将H2和N2按体积比3:1在密闭容器中混合,当该反应达到平衡时,测得平衡混合气中NH3的体积分数为,此时N2的转化率为______.
(3)某厂每天产生600m3含氨废水(NH3?的浓度为153mg?L-1,废氨水密度为1g?cm-3).该厂处理废水的方法:将废水加热得到NH3,使废水中NH3的浓度降为17mg?L-1.再对加热蒸发得到的NH3用一定量空气氧化.发生的主反应如下:
4NH3+5O24NO+6H2O?4NO+3O2+2H2O=4HNO3
副反应为:4NH3+3O2=2N2+6H2O
①该厂每天通过加热蒸发可得到NH3的物质的量是多少?
②若氧化过程中90%?NH3转化为硝酸,10%?NH3发生了副反应,则该厂每天消耗标准状况下的空气多少立方米?(假设废水加热前后的体积和密度近似认为不变,空气中氧气的体积分数20%.)
2、选择题 COCl2(g) CO(g)+Cl2(g);△H>0。当反应达到平衡时,下列措施:①升温;②恒容通入惰性气体;③增加CO的浓度;④减压;⑤加催化剂;⑥恒压通入惰性气体。能提高COCl2转化率的是
CO(g)+Cl2(g);△H>0。当反应达到平衡时,下列措施:①升温;②恒容通入惰性气体;③增加CO的浓度;④减压;⑤加催化剂;⑥恒压通入惰性气体。能提高COCl2转化率的是
[? ]
A.①②④
B.①④⑥
C.②③⑥
D.③⑤⑥
3、填空题 工业生产硝酸铵的流程图如下:?
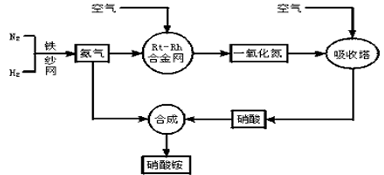
请回答下列问题:
(1)写出硝酸铵在工农业生产中的主要用途____________(任写一条)。
(2)已知N2 (g) +3H2(g) 2NH3(g) △H = -92kJ . mol-1。请回答:
2NH3(g) △H = -92kJ . mol-1。请回答:
①在500℃、 91exam.org200atm和铁催化条件下向一密闭容器中充入 1mol N2和3 mol H2,充分反应后,放出的热量_________(填 “<”“>”或“=”)92.4kJ,理由是_____________。
②为有效提高氢气的转化率,实际生产中宜采取的措施有___________
A.降低温度
B.最适合催化剂活性的适当高温
C.增大压强
D.降低压强
E.循环利用和不断补充氮气
F.及时移出氨
(3)写出氨在铂铑合金网催化氧化下的化学方程式:_________。
(4)在一定温度和压强的密闭容器中,将物质的量之比为 3:2的H2和N2混合,当该反应达到平衡时,测出平衡混合气中氨的体积分数为15%,此时H2的转化率为___________。
4、选择题 在一定温度下,将气体X和气体Y?各0.16mol充入10L?恒容密闭容器中,发生反应X(g)+Y(g)?2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表,下列说法不正确的是( )
| t/min | 2 | 4 | 7 | 9
n(Y)/mol
0.12
0.11
0.10
0.10
|
A.反应前2min的平均速率v(Z)=2.0×10-5?mol/(L?min)
B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2?mol?Z,平衡时X的体积分数增大
5、选择题 已知反应:2CH3COCH3(l) CH3COCH2COH(CH3)2(l)。取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y-t)如图所示。下列说法正确的是
CH3COCH2COH(CH3)2(l)。取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y-t)如图所示。下列说法正确的是
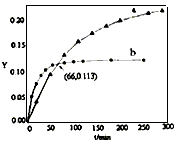
[? ]
A.b代表0℃下CH3COCH3的Y-t 曲线
B.反应进行到20min末,CH3COCH3的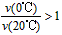
C.升高温度可缩短反应达平衡的时间并能提高平衡转化率
D.从Y=0到Y=0.113,CH3COCH2COH(CH3)2的