1、选择题 39号元素钇的电子排布式应是下列排布中的哪一种
A.1s22s22p63s23p63d104s24p64d15s2
B.1s22s22p63s23p63d104s24p65s25p1
C.1s22s22p63s23p63d104s24p64f15s2
D.1s22s22p63s23p63d104s24p65s25d1
2、填空题 现有X、Y、Z、W四种短周期元素原子序数依次增大,其原子半径及主要化合价如下表所示。又知X与Y、Z与W分别位于同一周期,Y、W处于同一主族。
元素
| X
| Y
| Z
| W
|
原子半径/nm
| 0.077
| 0.074
| 0.186
| 0.102
|
主要化合价
| -4,+4
| -2
| +1
| -2,+6
|
请回答:
小题1:X位于元素周期表的? ?,画出Z原子结构示意图? ?,
Z2W是离子晶体,写出其电子式? ?。
小题2:X单质能与某酸(H2WY4)的浓溶液发生反应,产物有XY2、WY2和水,
其反应的化学方程式为?;
小题3:Z2Y2可与XY2发生反应可给潜水艇供氧,其反应的化学方程式为?;
若反应中转移电子数为3.01×1023,则所得气体产物的体积是?(标准状况)。
小题4:Y、Z、W三种元素可组成质量比为5.75 : 8 : 4的某种化合物。实验室检验该化合物中所含阴离子的操作方法及有关实验现象是:取少量含该阴离子的溶液,?,则证明原溶液中含有该阴离子。
3、填空题 (14分)X、Y、Z、W、R是五种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y?元素原子的最外层电子数是其次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。请填写下列空白:
(1)画出W的原子结构示意图;?。
(2)Z和W最高价氧化物的水化物的碱性较强的是:?(写化学式),它们之间在溶液中反应的离子方程式是;?;
(3)Z2Y2 中阴离子的化学式是?。
(4)在同周期元素中,R 元素及与其相邻元素的原子半径从大到小的顺序是:?。与R元素同周期且非金属性最强的元素是:?。
(5)W的单质、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的化合物均由两种元素组成,且都是新型陶瓷材料,其反应的化学方程式是:?。
4、推断题 A、B、C、D、E、F为原子序数依次增大的短周期主族元素,已知A、C、F三种元素原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水;D元素原子的最外层电子数比次外层少4个;E元素原子次外层电子数比最外层多3个。
(1)写出下列元素的符号:A?, E?。
(2)A、C两种元素的最高价氧化物的水化物反应的离子方程式是?。
(3)A元素的最高价氧化物的水化物与C元素的最高价氧化物反应的化学方程式是?。
(4)与F元素处于同一主族的第四周期元素的基态原子核外电子排布式为?。
(5)用电子式表示B和F形成化合物的过程________________
5、选择题 X、Y、Z、W均为短周期元素,它们在周期表中的位置如图所示。若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是
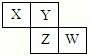
A.原子半径:W>Z>Y>X
B.相等物质的量浓度的气态氢化物溶液的pH: X>Z>W
C.最高价氧化物对应水化物的酸性:Z>W>X
D.四种元素的单质中,Z单质的熔沸点最低