1、选择题 向盛有KI溶液的试管中加适量溴水和四氯化碳,振荡后静置,可见到的现象是
A.上层为紫色液体,下层为无色液体
B.上层为无色液体,下层为紫色液体
C.均为紫色液体
D.上层为橙色液体,下层为紫色液体
参考答案:B
本题解析:CCl4比水重,I2的CCl4溶液为紫红色.
本题难度:一般
2、判断题 (10分)日常生活中有许多看似不显眼,却能够提供多种信息的材料,食品标签便是其中一种。
品名:×××梳打饼干
_________:小麦粉、食用植物油、麦芽糖、食盐、疏松剂、鸡全蛋粉、酵母、全脂奶粉、食用香精、酵母提取物、氟亚硫酸钠
净含量:400克
_________:九个月
生产日期:2006-04-17
保存方式:避免日晒,置阴凉干燥处
产品标准号:0/XOMR2
生产厂家:上海××饼干食品有限公司
地址:中国上海市××路××号
由编:200033
电话号码:(86-25)3414××××
|
(1)请将上边的食品标签补充完整。
(2)这包食品最迟应在_________之前食用。
(3)如果该食品有质量问题,你维权的办法是:
①_____________________________________________;
②___________________________。(可以只答一条)
参考答案:(1)配料(或成分、或原料)?保质期(或保存期)
(2)2007年1月17日
(3)向商家(厂家)退货或换货;向消费者权益保护委员会(或商检、质检部门)投诉
本题解析:(1)小麦粉、植物油、麦芽糖、食盐等属于饼干的成分或配料。
九个月应该是保质期。
(2)由生产日期2006-04-17后推9个月得2007-01-17,这包食品最迟应在该日前食用。
(3)可以要求调换、或退款,如果厂家或商家不同意,也可以向有关部门(如消协、商检、质检部门)投诉。
本题难度:简单
3、选择题 新制的饱和氯水与久置氯水的主要区别是
A.A
B.B
C.C
D.D
参考答案:B
本题解析:分析:根据新制的饱和氯水与久置氯水的成分.
解答:新制氯水的主要成分有:氯气,次氯酸、氯化氢,久置后主要成分有:氯化氢,即为盐酸;氯气能使湿润的淀粉KI试液变蓝,次氯酸是弱酸,具有漂白性、而盐酸是强酸,没有漂白性,也不能使淀粉KI试液变蓝,故选:B.
点评:本题主要考查了新制的饱和氯水与久置氯水的成分,难度不大.
本题难度:一般
4、选择题 下列食物中富含维生素的是
[? ]
A. 水果
B. 汽水
C. 甘蔗
D. 馒头
参考答案:A
本题解析:
本题难度:简单
5、选择题 Zn(OH)2是两性氢氧化物,和强酸反应时生成Zn2+,跟强碱反应时生成ZnO22-.现有三份等物质的量浓度、等体积的MgCl2、ZnCl2、AlCl3溶液(配制时均加入少量盐酸),现将一定浓度的NaOH溶液,分别滴入三种溶液中至过量,NaOH溶液的体积x(mL)与生成沉淀的物质的量y(mol)的关系如下图所示,则与MgCl2、ZnCl2、AlCl3三种溶液一一对应的正确图象是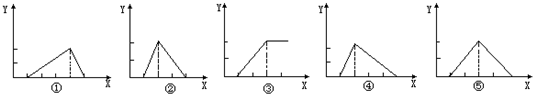
A.③②④
B.③⑤①
C.③⑤④
D.③②①
参考答案:B
本题解析:分析:等物质的量浓度、等体积的MgCl2、ZnCl2、AlCl3溶液,即三者的物质的量是相等的,将一定浓度的NaOH溶液,分别滴入三种溶液中至过量,所发生的反应过程如下:MgCl2+2NaOH=Mg(OH)2↓+2NaCl;ZnCl2+2NaOH=Zn(OH)2↓+2NaCl,Zn(OH)2↓+2NaOH=Na2ZnO2+2H2O;AlCl3+3NaOH=Al(OH)3↓+3NaCl,Al(OH)3↓+NaOH=NaAlO2+2H2O,根据溶液物质的量和化学方程式来确定沉淀的量.
解答:向氯化镁溶液中加入氢氧化钠,开始先中和其中的少量盐酸,然后生成白色沉淀氢氧化镁,当氢氧化钠过量时,沉淀也不会溶解,量保持不变,故对应的是图象③,向氯化锌溶液中加入氢氧化钠,开始先中和其中的少量盐酸,然后生成白色沉淀氢氧化锌,当氢氧化钠过量时,沉淀会溶解,依次发生反应ZnCl2+2NaOH=Zn(OH)2↓+2NaCl,Zn(OH)2↓+2NaOH=Na2ZnO2+2H2O,沉淀量达到最大和沉淀完全消失所消耗的氢氧化钠是相等的,故图象⑤是正确的,向氯化铝溶液中加入氢氧化钠,开始先中和其中的少量盐酸,然后生成白色沉淀氢氧化铝,当氢氧化钠过量时,沉淀会溶解,依次发生反应:
AlCl3+3NaOH=Al(OH)3↓+3NaCl,Al(OH)3↓+NaOH=NaAlO2+2H2O,沉淀量达到最大和沉淀完全消失所消耗的氢氧化钠的物质的量之比是3:1,故图象①是正确的.
故选B.
点评:本题考查学生金属镁、金属铝以及金属锌的可溶性盐溶液和强碱氢氧化钠之间的反应,属于化学反应知识的考查题,注意方程式的灵活应用是解题关键,难度不大.
本题难度:一般