1��ѡ���� �غ��Ƶ��������ƣ�����˵�����ܽϺõؽ��������ʵ���ǣ�������
A�����ǽ���Ԫ��
B��������������ͬ
C��ԭ�Ӱ뾶����
D������ϼ���ͬ
�ο��𰸣�A������Ԫ���кܶ��֣������ʲ���ȫ���ƣ�ֻ��λ��ͬһ�����Ԫ�أ����ʲ����ƣ���A����
B���ƺͼض�λ�����ڱ��ڢ����壬������������ͬ���������ƣ���B��ȷ��
C��ͬ����ԭ�Ӱ뾶���ϴ��������ƣ�ͬ����Ԫ��ԭ�Ӱ뾶�������ʲ�ͬ����C����
D�����ϼ���ͬ��Ԫ�����ʲ�һ����ͬ����Mg��Cu����ϼ۶�Ϊ+2�ۣ������ʲ�ͬ����D����
��ѡB��
���������
�����Ѷȣ���
2������� A��B��C��D���Ƕ�����Ԫ�أ�ԭ�Ӱ뾶��D��C��A��B����֪��A��Bͬ���ڣ�A��C����ͬһ���壻Cԭ�Ӻ��ڵ�����������A��Bԭ�Ӻ��ڵ�������֮�ͣ�Cԭ��������������Dԭ��������������3�����Իش�
��1��д��Ԫ�ص����ƣ�A______��C______��
��2��д����B��D��ɵ����ֻ�����ĵ���ʽ�ֱ�Ϊ��______��______��
��3��C�Ĺ�̬����������______���壮д����ʾC���������һ����Ҫ�Ĺ�ҵ��;______��
��4��A��C������������Ӧˮ���������Խ�ǿ����______��дˮ����ķ���ʽ����
��5��д��C����������D������������Ӧˮ���ﷴӦ�����ӷ���ʽ______��
�ο��𰸣���A��Cͬ���壬ԭ�Ӱ뾶C��A����A��C���������8��Cԭ�Ӻ��ڵ�����������A��Bԭ�Ӻ��ڵ�������֮�ͣ��Ƴ�Bԭ�ӵ�������Ϊ8����BΪOԪ�أ�CΪ��������Ԫ�أ���Cԭ��������������Dԭ��������������3������D�����Ϊ1�����ӣ���C�����Ϊ3�����ӣ���D�������2�����ӣ���C�������6�����ӣ���C��B��ͬ����Ԫ���ˣ����������⣬��CΪAlԪ�أ�DΪNaԪ�أ�AΪBԪ�أ�
��1��AΪBԪ�أ�CΪAlԪ�أ��ʴ�Ϊ��������
��2����B��D��ɵ����ֻ�����ֱ�ΪNa2O��Na2O2�����������ӻ��������ʽ�ֱ�Ϊ
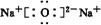
��
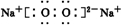
��
�ʴ�Ϊ��
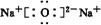
��
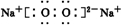
��
��3��CΪAlԪ�أ���Ӧ��������ΪAl2O3��Ϊ���ӻ�����۵�ߡ�Ӳ�ȴ������ͻ���ϣ�Ҳ�����ڵ��ұ������ԭ�ϣ��ʴ�Ϊ�����ӣ����ͻ���ϻ���ұ������
��4��A��C������������Ӧˮ����ֱ�ΪH3BO3��Al��OH��3������H3BO3ΪһԪ�ᣬAl��OH��3Ϊ���������������ǿ����H3BO3���ʴ�Ϊ��H3BO3��
��5��Al2O3Ϊ�������������NaOH��Һ��Ӧ����Ӧ�����ӷ���ʽΪ���ʴ�Ϊ��Al2O3+2OH-+3H2O�T2[Al��OH��4]-��
���������
�����Ѷȣ�һ��
3������� ���мס�������Ԫ�أ���3����Ԫ�ؼ��������2�����ӣ�Ԫ����3p�ܼ��ϵĵ����Ų���ʽΪ

(1)д���ס�����Ԫ�صķ��ţ���_______����_______��
(2)�ס�����Ԫ���γɵĵ��ʼ��ȷ�Ӧ��IJ�����_____����Ϊ_______ ������ӡ����ۡ�����������Ƿ�����Ӧ�Ļ�ѧ����ʽΪ_________________��
�ο��𰸣�(1)Mg��S
(2)MgS�����ӣ�Mg+S MgS
MgS
���������
�����Ѷȣ�һ��
4��ѡ���� A��B��C��D�������ڱ���ǰ20��Ԫ�أ���֪A�������Ӻ�C�������Ӿ�����ͬ�ĺ�������Ų��������γ����ΪAC�Ļ����C��D��ͬ���壬����C�ĺ����������D�ĺ�����������2����B��D��ͬ����Ԫ����A��B���γ�AB2�ͻ��������˵������ȷ���ǣ�������
A��DԪ�ش���Ԫ�����ڱ��еڶ����ڢ���
B��BC2����һ���Ǽ��Է���
C��AB2�п��ܼ������Ӽ����й��ۼ�
D������Ԫ�ص�ԭ�Ӱ뾶��Сһ����A��C��D��B
�ο��𰸣��⣻C��D��ͬ���壬����C�ĺ����������D�ĺ�����������2������CΪSԪ�أ�DΪOԪ�أ�A�������Ӻ�C�������Ӿ�����ͬ�ĺ�������Ų��������γ����ΪAC�Ļ������A�����ڱ��������ڣ��ڢ�A�壬ӦΪCaԪ�أ�B��D��ͬ����Ԫ����A��B���γ�AB2�ͻ������BΪCԪ�ػ�FԪ�أ��γɵĻ�����ΪCaF2��CaC2��
A��DΪOԪ�أ�����Ԫ�����ڱ��еڶ����ڢ�A�壬��A����
B����BC2����ΪCS2��Ϊֱ���η��ӣ��ṹ�Գƣ��ǷǼ��Է��ӣ���B����
C����AB2��CaC2����������Ӽ����й��ۼ�����C��ȷ��
D����B��CԪ�أ�������Ԫ�ص�ԭ�Ӱ뾶��С˳����A��C��B��D����D����
��ѡC��
���������
�����Ѷȣ�һ��
5������� A��B��C��D�����ֶ�����Ԫ�أ�E��F�ǹ���Ԫ�أ�A��B��Cͬ���ڣ�C��Dͬ���壬A��ԭ�ӽṹʾ��ͼΪ��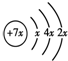 ��B��ͬ���ڳ�ϡ��������뾶����Ԫ�أ�C��������������ɵ����ӣ�E��F����Χ�����Ų�ʽ�ֱ�Ϊ3d54s1��3d64s2���ش��������⣺
��B��ͬ���ڳ�ϡ��������뾶����Ԫ�أ�C��������������ɵ����ӣ�E��F����Χ�����Ų�ʽ�ֱ�Ϊ3d54s1��3d64s2���ش��������⣺
��1��A�Ļ�̬ԭ�ӵĵ����Ų�ʽ��______��
��2��B�����������Ļ�ѧʽΪ______��C��������ϼ�Ϊ______��
��3���ù����ʾʽ��ʾDԭ�Ӻ�������Ų�______��
��4������ΪʲôE����Χ�����Ų�ʽΪ3d��54s1������Ϊ3d44s2��______��
��5��Fԭ�ӽṹʾ��ͼ��______��
�ο��𰸣�A��B��C��D�����ֶ�����Ԫ�أ�A��ԭ�ӽṹʾ��ͼΪ�� ��x=2����AΪSiԪ�أ�A��B��Cͬ���ڣ����ڵ������ڣ�B��ͬ���ڳ�ϡ��������뾶����Ԫ�أ�BΪNaԪ�أ�C��������������ɵ����ӣ���Χ�����Ų�Ϊ3s23p3����CΪPԪ�أ�C��Dͬ���壬��DΪNԪ�أ�E��F�ǹ���Ԫ�أ�E��F����Χ�����Ų�ʽ�ֱ�Ϊ3d54s1��3d64s2����EΪCrԪ�أ�FΪFeԪ�أ�
��x=2����AΪSiԪ�أ�A��B��Cͬ���ڣ����ڵ������ڣ�B��ͬ���ڳ�ϡ��������뾶����Ԫ�أ�BΪNaԪ�أ�C��������������ɵ����ӣ���Χ�����Ų�Ϊ3s23p3����CΪPԪ�أ�C��Dͬ���壬��DΪNԪ�أ�E��F�ǹ���Ԫ�أ�E��F����Χ�����Ų�ʽ�ֱ�Ϊ3d54s1��3d64s2����EΪCrԪ�أ�FΪFeԪ�أ�
��1��AΪSiԪ�أ�ԭ�Ӻ��������Ϊ14����̬ԭ�ӵĵ����Ų�ʽ�ǣ�1s22s22p63s23p2���ʴ�Ϊ��1s22s22p63s23p2��
��2��BΪNaԪ�أ����������Ļ�ѧʽΪ��Na2O��CΪPԪ�أ�����������Ϊ5��������ϼ�Ϊ-3���ʴ�Ϊ��Na2O��-3��
��3��DΪNԪ�أ�ԭ�Ӻ��������Ϊ7��������ӹ����ʾΪ��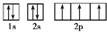 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��4��E����Χ���ӳ�3d��54s1ʱ��3d��4s����ϵĵ��Ӵ��ڰ���״̬��������ϵ��������ͣ���ôE����Χ�����Ų�ʽΪ3d��54s1������Ϊ3d44s2��
�ʴ�Ϊ��E����Χ���ӳ�3d��54s1ʱ��3d��4s����ϵĵ��Ӵ��ڰ���״̬��������ϵ��������ͣ�
��5��FΪFeԪ�أ���26��Ԫ�أ�Feԭ�ӽṹʾ��ͼ�ǣ�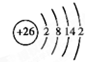 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
���������
�����Ѷȣ�һ��