1、选择题 某主族元素的原子,M层上有一个半充满的能级,这种原子的质子数是
[? ]
A.只能是7
B.只能是15
C.是11或15
D.是11或13
参考答案:C
本题解析:
本题难度:简单
2、选择题 同一横行X、Y、Z三种元素,已知最高价氧化物对应的水化物的酸性是HXO4>H2YO4>H3ZO4,则下列说法判断错误的是( )
A.原子半径 X>Y>Z
B.元素的非金属性 X>Y>Z
C.气态氢化物稳定性 HX>H2Y>ZH3
D.单质的氧化性 X>Y>Z
参考答案:X、Y、Z三种元素位于周期表同一周期,最高价氧化物对应的水化物的酸性是 HXO4>H2YO4>H3ZO4,可说明非金属性X>Y>Z,因同周期元素从左到右元素的非金属性逐渐增强,则原子序数X>Y>Z,
A.X、Y、Z三种元素位于周期表同一周期,原子序数X>Y>Z,原子半径逐渐减小,故A错误;
B.由以上分析可知元素的非金属性 X>Y>Z,故B正确;
C.非金属性 X>Y>Z,元素的非金属性越强,对应的氢化物越稳定,故C正确;
D.非金属性 X>Y>Z,元素的非金属性越强,对应的单质的氧化性越强,故D正确.
故选A.
本题解析:
本题难度:一般
3、选择题 下列关于S元素的描述正确的是( )
A.它与H2生成液态化合物一定不存在分子间氢键
B.原子的电负性同周期最高
C.它的外围电子排布式为1s22s22p63s23p4
D.其电子排布图为: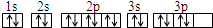
参考答案:A.硫和氢气反应生成硫化氢,硫化氢中硫元素电负性较小,所以不存在氢键,故A正确;
B.与硫同周期的元素中,氯元素的电负性大于硫,故B错误;
C.硫原子的外围电子排布式为3s23p4,故C错误;
D.该电子排布图违反了洪特规则,故D错误;
故选A.
本题解析:
本题难度:一般
4、选择题 有a、b、c、d四种元素.a、b的阳离子与c、d的阴离子具有相同的电子层结构;a的阳离子的正电荷数小于b的阳离子的正电荷数,c的阴离子的负电荷数大于d的阴离子的负电荷数.则它们的离子半径的关系是( )
A.a>b>c>d
B.c>d>a>b
C.c>a>d>b
D.b>a>d>c
参考答案:a、b的阳离子与c、d的阴离子具有相同的电子层结构,则a、b在下一周期的前方,c、d在上一周期的后方;
a的阳离子的正电荷数小于b的阳离子的正电荷数,则原子序数b>a;
c的阴离子的负电荷数大于d的阴离子的负电荷数,则原子序数d>c,
所以原子序数为b>a>d>c,
由具有相同电子层结构的离子,原子序数大的离子半径小,
则离子半径为c>d>a>b,
故选B.
本题解析:
本题难度:简单
5、选择题 下列四种元素中,其单质氧化性最强的是( )
A.原子含有未成对电子最多的第二周期元素
B.位于周期表中第三周期ⅢA族的元素
C.原子最外电子层排布为2s22p6的元素
D.原子最外电子层排布为3s23P5的元素
参考答案:D
本题解析:
本题难度:简单