1、选择题 已知中学化学中常见反应形式为: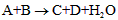 ,对于该反应的下列叙述不正确的是
,对于该反应的下列叙述不正确的是
[? ]
A.该反应可能是氧化还原反应
B.该反应可能是非氧化还原反应
C.C和D有一种一定是盐
D.A和B不一定是酸或碱
2、填空题 氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。
(1)水是人体的重要组成成分,是人体中含量最多的一种物质。而“四种基本反应类型
与氧化还原反应的关系”也可用如图表达。
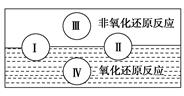
试写出有水参加的符合反应类型Ⅳ的一个化学方程式:________________________,其中水为________剂。
(2)氯化铵常用作焊接。如:在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为:
CuO+____NH4Cl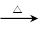 Cu+____CuCl2+N2↑+____H2O。
Cu+____CuCl2+N2↑+____H2O。
①配平此氧化还原反应方程式。
②该反应中,被氧化的元素是________(填元素名称),氧化剂是________(填化学式)。
(3)(2011・福建高考卷节选)磷酸钙与焦炭、石英砂混合,在电炉中加热到1 500 ℃生成白磷,反应为:
2Ca3(PO4)2+6SiO2=6CaSiO3+P4O10,10C+P4O10=P4+10CO。
每生成1 mol P4时,就有________mol电子发生转移。
3、选择题 已知反应:①Cl2+2KBr=2KCl+Br2, ②KClO3 +6HCl=3Cl2+KCl +3H2O,
③2KBrO3 +Cl2=Br2 + 2KClO3,下列说法正确的是
A.上述三个反应都有单质生成,所以都是置换反应
B.氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2
C.反应②中还原剂与氧化剂的物质的量之比为6:1
D.③中lmol还原剂反应则氧化剂得到电子的物质的量为2mol
4、选择题 下列叙述正确的是
[? ]
A.分解反应一定是氧化还原反应
B.氧化还原反应的特征:化合价发生变化
C.还原剂就是反应中被还原的物质
D.在氧化还原反应中,失去电子的元素化合价降低
5、选择题 用0.1 mol・L-1的Na2SO3溶液30 mL恰好将2×10-3 mol的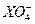 还原,则元素X在还原产物中的化合价是(?)
还原,则元素X在还原产物中的化合价是(?)
A.+1
B.+2
C.+3
D.+4