|
高考化学知识点总结《物质结构和元素周期律》高频试题强化练习(2017年最新版)(二)
2017-11-11 04:17:18
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
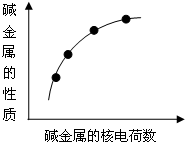
1、选择题 右图表示碱金属的某些性质与核电荷数的变化关系,下列各性质中不符合图示关系的是( )
A.还原性
B.与水反应的剧烈程度
C.熔点
D.原子半径
| 
参考答案:A.碱金属元素中,随着碱金属的核电核数的增大,元素的金属性逐渐增强,单质的还原性逐渐增强,故A正确;
B.碱金属元素中,随着碱金属的核电核数的增大,元素的金属性逐渐增强,与水反应的剧烈程度逐渐增大,故B正确;
C.碱金属元素中,随着碱金属的核电核数的增大,金属晶体的金属键作用力减弱,熔点逐渐降低,故C错误;
D.碱金属元素中,随着碱金属的核电核数的增大,核外电子层数逐渐增多,电子层数越多,半径越大,故D正确.
故选C.
本题解析:
本题难度:简单
2、选择题 下列说法都正确的是
[? ]
①江河入海口三角洲的形成通常与胶体的性质有关
②四川灾区重建使用了大量钢材,钢材是合金
③“钡餐”中使用的硫酸钡是弱电解质
④太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置
⑤常用的自来水消毒剂有氯气和二氧化氮,两者都含有极性键
⑥水陆两用公共汽车中,用于密封的橡胶材料是高分子化合物
A.①②③④
B.①②④⑥
C.①②⑤⑥
D.③④⑤⑥
参考答案:B
本题解析:
本题难度:简单
3、选择题 X元素的阳离子与Y的阴离子具有相同的核外电子排布,则下列比较中正确的是
A.原子序数: X< Y
B.原子半径:X< Y
C.离子半径:X> Y
D.最外层电子数:X< Y
参考答案:D
本题解析:试题分析:X元素的阳离子与Y的阴离子具有相同的核外电子排布,这说明X是金属元素,Y是非金属元素,位于X的上一周期。则原子序数是X>Y,A不正确;原子半径是X>Y,B不正确;核外电子排布相同的微粒,其微粒半径随原子序数的增大而减小,所以离子半径是X<Y,C不正确。一般金属元素的核外电子数小于非金属元素的核外电子数,因此正确的答案选D。
考点:考查核外电子排布、元素周期表的结构以及元素周期律的应用
点评:该题是中等难度的试题,试题贴近高考,侧重对学生能力的培养和解题方法的指导与训练,旨在培养学生灵活运用基础知识解决实际问题的能力。该题的关键是明确元素周期表的结构特点,然后结合题意灵活运用即可,有利于培养学生的逻辑推理能力。
本题难度:简单
4、选择题 下列各组元素性质递变规律正确的是( )
A.Na、Mg、Al原子半径依次减小
B.Li、Be、B原子最外层电子数依次减小
C.P、S、Cl元素最高正价依次降低
D.Li、Na、K的金属性依次减弱
参考答案:A.Na、Mg、Al位于同一周期,根据同周期元素从左到右原子半径逐渐减小,则原子半径:Na>Mg>Al,故A正确;
B.Li、Be、B最外层电子数依次为1、2、3,最外层电子逐渐增多,故B错误;
C.P、S、Cl最外层电子数分别为5、6、7,最高化合价依次为+5、+6、+7,最高正价依次升高,故C错误;
D.Li、Na、K位于同一主族,同主族元素从上到下元素的金属性逐渐增强,则金属性:Li<Na<K,故D错误.
故选A.
本题解析:
本题难度:简单
5、填空题 下表是元素周期表中短周期元素部分,表中字母分别代表一种元素:
(1)上述______元素(填元素名称)可以形成硬度最大的单质.
(2)“神舟”六号飞船内需要有一种化合物来吸收宇航员呼出的?CO2,并释放出O2,你认为该物质应该是由上表中的______和______元素(填元素名称)组成的.飞船中需要制造一种适合宇航员生存的人工生态环境,应该在氧气中充入一种气体用于稀释氧气,该气体分子是______.
(3)表中元素g的氢化物稳定性比元素e的氢化物的稳定性______(填“强”或“弱”).
(4)将潮湿的由h元素构成的单质通过甲装置后,再通过放有干燥红色布条的乙装置,红色布条不褪色.则甲装置中所盛试剂可能是______.
①浓硫酸?②NaOH溶液
③KI溶液?④饱和食盐水
(5)写出h元素构成的单质与水反应的化学方程式:______.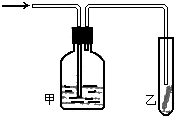
参考答案:根据元素周期表的结构,可推知a是H,b是He,c是Na,d是C,e是N,f是O,g是Si,h是Cl.
(1)碳元素的单质金刚石是自然界硬度最大的单质,故答案为:碳;
(2)过氧化钠和二氧化碳反应生成氧气,为稀释氧气,制造一种适合宇航员生存的人工生态环境,可以在飞船中加氮气,制造类似空气的环境,故答案为:钠、氧、N2;
(3)根据元素周期律:同一周期从左到右,氢化物的稳定性增强,同主族从上到下,氢化物的稳定性减弱,所以元素N的氢化物稳定性比元素Si的氢化物的稳定,故答案为:弱;
(4)干燥的氯气不能使红色布条褪色,所以①中放的试剂可能将氯气干燥,或者直接和氯气反应了,即为浓硫酸或氢氧化钠或是碘化钾,故答案为:①②③;
(5)氯气和水的反应为:Cl2+H2O=HCl+HClO,故答案为:Cl2+H2O=HCl+HClO.
本题解析:
本题难度:简单
| 
