1、选择题 短周期元素甲、乙、丙、丁、戊五种元素在元素周期表中的位置如下图所示,其中戊是同周期中原子半径最小的元素。下列有关判断正确的是( )
A.最外层电子数:甲>乙>丙>丁>戊
B.简单离子的离子半径:戊>丁>丙
C.含有丁元素的酸有多种
D.乙的氢化物多种多样,丙、丁、戊的氢化物各有一种
参考答案:C
本题解析:戊是同周期中原子半径最小的元素,则戊是Cl,所以丁是S,丙是N,乙是C,甲是B。同周期自左向右最外层电子数逐渐最多,A不正确。核外电子排布相同的微粒,其微粒半径随原子序数的增大而减小,因此B中应该是丁>戊>丙,B不正确。C正确,例如硫酸、亚硫酸、氢硫酸等。N的氢化物不止一种,例如氨气、N2H4等,D不正确,答案选C。
本题难度:简单
2、填空题 Ⅰ. A、B、C、D、E、F、G七种元素,试按下列所给条件推断,
①A、B、C是同一周期的金属元素,原子核外有三个电子层,A的原子半径在所属周期中最大,且原子半径A>B>C;
②D、E是非金属元素,它们跟氢气化合可生成气态氢化物HD和HE,室温时,D的单质是液体,E的单质是固体
③F在常温下是气体,性质稳定,是除氢气外最轻的气体
④G是除氢外原子半径最小的元素
(1)A 的名称是?,B位于周期表中第?周期第?族。
(2)C的原子结构示意图是?,
A元素与D元素形成化合物的电子式是?。
(3)F的元素符号是?。
(4)在上述七种元素中,最高价氧化物对应的水化物碱性最强的化学式是?,酸性最强的化学式是?,气态氢化物最稳定的化学式是?。
(5)将C的氧化物对应的水化物投入到A的氧化物对应的水化物中,反应的化学方程式是
?。
Ⅱ、(1)下表中的实线表示元素周期表部分边界,请用实线画出周期表未完成的边界及金属元素与非金属元素的分界线。
?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
(2)把符合下列要求的元素的元素符号标在表中对应位置处。
① 最高价氧化物的水化物碱性最强(放射性元素除外)
② 气态氢化物最稳定的非金属元素
参考答案:(1)钠(1分) 三?ⅡA (1分)
(2)铝原子结构示意图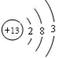 (1分)溴化钠电子式
(1分)溴化钠电子式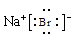 (1分)
(1分)
(3)He (1分)?
(4)? NaOH (1分)? HBrO4 (1分)? HF? (1分)
(5)Al(OH)3+NaOH =NaAlO2+2H2O (3分)
Ⅱ、边界(1分)分界线(1分) F(1分) Cs(1分)

本题解析:在同周期中,原子半径随原子序数的增大而减小。据题意可知A为钠B为镁C为铝。由室温时,D的单质是液体,E的单质是固体可知D为溴、E为硫.由F在常温下是气体,性质稳定,是除氢气外最轻的气体可知F应为氦。由G是除氢外原子半径最小的元素可知G应为氟。
本题难度:一般
3、简答题 【物质结构与性质】
X、Y、Z、M、N、Q为元素周期表前四周期的六种元素。其中X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,M的内层电子数是最外层电子数的9倍,N的原子序数比M小1, Q在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X元素在周期表中的位置是?,属??区元素,它的最外层电子的电子排布图为?。
(2)XZ2分子的立体结构是?,YZ2分子中Y的杂化轨道类型为?,相同条件下两者在水中的溶解度较大的是?(写分子式),理由是 ?。
(3)含有元素N的盐的焰色反应为?色,许多金属盐都可以发生焰色反应,其原因是?。
(4)元素M与元素Q形成晶体结构如图所示,设其晶胞边长为a pm,则a位置与b位置之间的距离为_______pm(只要求列算式)。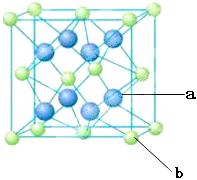
参考答案:(1)第三周期ⅥA族? P ?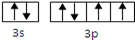
(2)V? sp? SO2? SO2为极性分子,CO2为非极性分子,H2O为极性溶剂,极性分子易溶于极性溶剂,故SO2的溶解度较大。
(3)紫?电子由较高能级跃迁到较低能级时,以光的形式释放能量。
(4)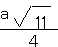
本题解析:第三周期ⅥA族,X、Y、Z、M、N、Q为元素周期表前四周期的六种元素,X原子核外的M层中只有两对成对电子,核外电子排布应为1s22s22p63s23p4,X为S元素;Y原子核外的L层电子数是K层的两倍,Y有2个电子层,最外层电子数为4,故Y为C元素;Z是地壳内含量最高的元素,为O元素;M的内层电子数是最外层电子数的9倍,M只能处于第四周期,最外层电子数只能为2,内层电子总数为18,核外电子总数为20,故M为Ca元素;N的原子序数比M小1,则N为K元素;Q在元素周期表的各元素中电负性最大,Q为F元素。
(1)X为S元素,元素在周期表中的位置是:第三周期ⅥA族,外围电子排布为3s23p4,最后1个电子填充p能级,属于p区元素,它的外围电子的电子排布图为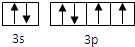 。
。
(2)SO2分子中S原子价层电子对数=2+(6-2×2)/2=3,S原子含有1对孤电子对,故其立体结构是V型,CO2分子C原子呈2个σ键、没有孤电子对,C的杂化轨道类型为sp杂化,SO2为极性分子,CO2为非极性分子,H2O为极性溶剂,极性分子易溶于极性溶剂,故SO2的溶解度较大。
(3)含有K元素的盐的焰色反应为紫色,许多金属盐都可以发生焰色反应,其原因是电子由较高能级跃迁到较低能级时,以光的形式释放能量。
(4)
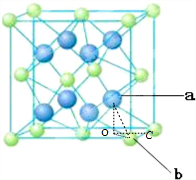
上下方向的平面:晶胞上底面、下底面、中间4个绿色球构成的平面、8个蓝色球构成立方体的上底面、下底面,这5个面之间的距离相等为 a pm,同理,左右方向形成的面间的距离相等为
a pm,同理,左右方向形成的面间的距离相等为 a pm,故a球到晶胞右侧面的距离为
a pm,故a球到晶胞右侧面的距离为 apm,到晶胞前面距离为
apm,到晶胞前面距离为 a pm,从a球向晶胞下底面作垂线,垂足为o,再作oc垂直棱,即oc为
a pm,从a球向晶胞下底面作垂线,垂足为o,再作oc垂直棱,即oc为 a pm,bc长为
a pm,bc长为 a pm,ao长为
a pm,ao长为 a pm,ab两球的距离=
a pm,ab两球的距离=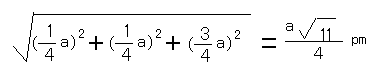
本题难度:一般
4、选择题 X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示。若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是(? )
 ?
?
A.只由这四种元素不能组成有机化合物
B.最高价氧化物对应水化物的酸性W比Z弱
C.Z的单质与氢气反应较Y剧烈
D.X与Y形成的化合物都易溶于水
参考答案:A
本题解析:Y原子的最外层电子数是内层电子数的3倍,所以Y为氧。根据图表,X为氮,Z为硫,W为氯。没有碳元素,所以不能组成有机化合物。W比Z非金属性强,所以最高价氧化物对应水化物的酸性W比Z强。Y的非金属性强于Z,所以Y的单质与氢气反应较Z剧烈。.X与Y形成的化合物不都易溶于水,如:NO。
本题难度:简单
5、填空题 下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
?
| ⅠA
| ⅡA
| ⅢA
| ⅣA
| ⅤA
| ⅥA
| ⅧA
| 0
|
二
| ?
| ?
| ?
| ?
| ①
| ?
| ②
| ?
|
三
| ③
| ④
| ⑤
| ⑥
| ?
| ?
| ⑦
| ⑧
|
四
| ⑨
| ?
| ?
| ?
| ?
| ?
| ⑩
| ?
|
(1)在这些元素中,最易失电子的元素是?,非金属性最强的元素是? ?;
(2)化学性质最不活泼的元素是? ?,其原子的原子结构示意图为? ?
(3)元素的最高价氧化物对应的水化物中酸性最强的是?,呈两性的氢氧化物是?。
参考答案:(每空1分,共6分)(1)K,F(2)Ar, (3)HClO4, Al(OH)3
(3)HClO4, Al(OH)3
本题解析:(1)根据元素在周期表中的位置可知,⑨的金属性最强,因此最容易失去电子的元素是K;同样分析可知,非金属最强的是②,即为F元素。
(2)化学性质最不活泼的元素是稀有气体元素,即⑧,是Ar,其原子结构示意图是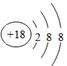 。
。
(3)非金属性越强,最高价氧化物的水化物的酸性越强,则酸性最强的是HClO4;而呈两性的氢氧化物是氢氧化铝。
点评:该题是高考中的常见考点,属于基础性试题的考查。侧重对学生基础知识的巩固与训练,有助于培养学生的逻辑推理能力。本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识和灵活运用知识的能力。该题以“周期表中元素的推断”为载体,考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。
本题难度:一般