| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点总结《气体的净化、干燥、吸收与收集》试题特训(2017年最新版)(六)
(2)该小组同学设计的制备氮化镁的实验方案如下图 (夹持及加热仪器没有画出),且在实验前系统内的空气均已排尽。 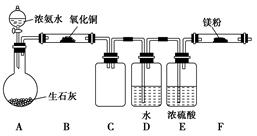 ①该实验完成后,能否得到纯净的氮化镁________(填“能”或“不能”);简述理由____________________________________________________。 ②装置C的作用是___________________________________. 参考答案:(1)AB (NH4)2SO4+Ca(OH)2CaSO4+2NH3↑+2H2O; NH3・H2ONH3↑+H2O 本题解析:略 本题难度:一般 2、选择题 如图装置可用于收集气体并验证其某些化学性质(不考虑烧杯中液体倒吸现象),你认为正确的是( )
A.A B.B C.C D.D |

参考答案:A.二氧化硫和澄清的石灰水反应生成难溶于水的亚硫酸钙和水,出现浑浊现象与二氧化碳与澄清的石灰水反应的现象相同,所以A选项中不能判断X为二氧化硫,故A错误;
B.氯气和紫色的石蕊作用先显红色,是由于氯气和水反应生成盐酸和次氯酸,酸使紫色的石蕊试液变红,后来褪色,是由于生成的次氯酸具有强氧化性和漂白性,所以褪色,氯气没有漂白性,故B错误;
C.二氧化氮和水反应生成硝酸和一氧化氮,发生3NO2+H2O=2HNO3+NO↑,生成的硝酸具有强氧化性将KI淀粉溶液中的碘离子氧化成碘单质,碘单质和淀粉作用显示蓝色,所以说NO2水溶液有氧化性正确,故C正确.
D.如图装置是可用于收集气体并验证其某些化学性质的,如果收集氨气,氨气的密度比空气小,需短管进,长管出,故D错误;
故选C.
本题解析:
本题难度:一般
3、实验题 (14分) 某小组准备在实验室中制取干燥、纯净的氯气并验证氯气的性质,设计了如下的实验装置图:
(一) 制取纯净的氯气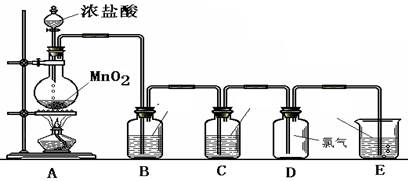
(1)?写出A中反应的化学方程式:____________________________________.
(2)?B中加入的物质是:___________________作用是:___________________.
(3)?C中加入的物质是:___________________作用是:___________________.
(4)?E中反应方程式为:_____________________________________________.
(二) 验证氯气的性质:
(5)?B中发生反应的方程式为:_______________________________________.
(6)?C中发生反应的方程式为:______________________________________.
(7)?D中的反应方程式为:__________________________________________.
参考答案:(1) MnO2 + 4HCl =MnCl2 +Cl2 + H2O
(2) 饱和食盐水?除去Cl2中混有的HCl气体
(3) 浓硫酸?干燥Cl2
(4) 2NaOH + Cl2 =" NaCl" + NaClO +H2O
(5) Cl2 +2KI ="2KCl" + I2
(6) Cl2 +Na2SO3+ H2O = Na2SO4 + 2HCl
(7) 2FeCl2 +Cl2=2FeCl3
本题解析:略
本题难度:一般
4、实验题 已知实验室制取H2S的实验原理为FeS(块状)+H2SO4===FeSO4+H2S↑。根据下图中A~D 的实验装置和试剂进行实验:
(1)装置A是由双孔塞、玻璃导管、________和________组装起来的。
(2)组装一套制取二氧化硫气体的装置,并证明二氧化硫既有氧化性又有还原性: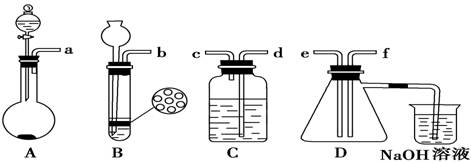
制备SO2的实验原理:Na2SO3(粉末状)+H2SO4(70%)===Na2SO4+SO2↑+H2O。
①按实验装置连接顺序:把a→f各导管口连接起来,正确的顺序是___________。
②C装置中的溶液是 ,说明二氧化硫具有 性。
(3)D中产生的现象是 ,说明二氧化硫具有 性。
(4)烧杯中发生反应的离子方程式为________________________。
参考答案:(1)圆底烧瓶 分液漏斗 (2分)(2)①a→d→c→e→f→b(f和e可以互换)(2分) ②溴水(或酸性高锰酸钾溶液) (2分)还原(1分)
(3)有淡黄色物质附着在反应容器内壁(2分) 氧化(1分) (4)SO2+2OH-===SO32-+H2O,H2S+2OH-===S2-+2H2O (2分)
本题解析:略
本题难度:一般
5、选择题 下列气体中既不能用浓硫酸干燥,又不能用固体NaOH干燥的是
[? ]
A.Cl2
B.O2
C.SO2
D.H2S
参考答案:D
本题解析:
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点总结《物质的量浓.. | |