1、填空题 (8分)已知有以下物质相互转化

试回答:(1)写出B的化学式?,D的化学式?。
(2)写出由E转变成F的化学方程式?。
(3)写出F转化成G的离子方程式?;
2、填空题 实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4・7H2O),过程如下:

(1)将过程②中的产生的气体通入下列溶液中,溶液会褪色的是__________;
A.品红溶液? B.紫色石蕊溶液?C.酸性KMnO4溶液? D.溴水
(2)过程①中,FeS和O2、H2SO4反应的化学方程式为:___________________________________。
(3)过程③中,需加入的物质是___________________________。
(4)过程④中,蒸发结晶需要使用酒精灯、三角架、泥三角,还需要的仪器有_______________。
(5)过程⑤调节pH可选用下列试剂中的___________ (填选项序号);
A.稀硫酸? B.CaCO3? C.NaOH溶液
(6)过程⑥中,将溶液Z加热到70一80℃,目的是_____________________。
(7)实验室为测量所得到的聚铁样品中铁元素的质量分数,进行下列实验。①用分析天平称取2.70g样品;②将样品溶于足量的盐酸后,加入过量的氯化钡溶液;③过滤、洗涤、干燥,称量,得固体质量为3.495g。若该聚铁主要成分为[(Fe(OH)(SO4)]n,则该聚铁样品中铁元素的质量分数为___________。(假设杂质中不含铁元素和硫元素)。
3、填空题 有一种细菌在酸性水溶液、氧气存在下,可以将黄铜矿(主要成分是CuFeS2,含少量杂质SiO2)氧化成硫酸盐。运用该原理生产铜和绿矾(FeSO4・7H2O)的流程如下: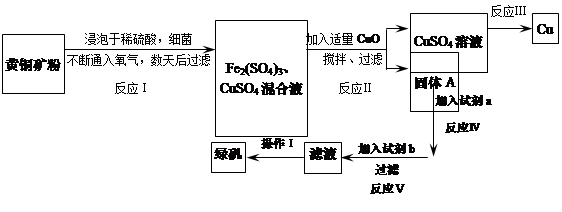
回答下列问题:
(1)已知:
?
| Fe2+
| Cu2+
| Fe3+
|
开始转化成氢氧化物沉淀时的pH
| 7.6
| 4.7
| 2.7
|
完全转化成氢氧化物沉淀时的pH
| 9.6
| 6.7
| 3.7
|
?
(1)加入CuO将溶液的pH调节到约为4,结合平衡移动原理解释该操作的原因?。
(2)写出能实现反应Ⅲ的化学方程式?。
(3)试剂b为?。
(4)欲从滤液中获得绿矾晶体,操作Ⅰ应为浓缩、?、?。
(5)反应Ⅰ的化学方程式?。
4、选择题 (13分)某研究性学习小组的同学利用下图来验证某铜银合金完全溶解于浓硝酸时生成的气体除NO2外还含有NO,并测定合金中铜的质量分数。已知常温下NO2和N2O4混合存在,在低于0℃时几乎只有无色的N2O4晶体。
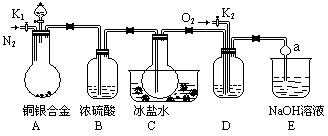
(1)写出A中铜与硝酸反应的一个化学方程式_________________________________
(2)反应前先打开A部分的活塞K1,持续通入一段时间的N2,理由是_________________
若装置中缺少B部分,会影响验证的结果,其原因是___________________________
(3)反应结束后,打开活塞K2,并通入O2,若有NO产生,则D产生的现象是________
_______________________
(4)实验测得的数据如下:合金质量15.0g,13.5mol/LHNO340mL;实验后A溶液:V=40mL,c(H+)=1.0mol/L,假设反应中硝酸无挥发也没有分解。则反应中消耗的HNO3物质的量为_____mol;
(5)利用A装置中反应后溶液也可确定铜的质量分数,方法是取出A中的反应的溶液,向其中加入足量的_____溶液,然后进行的操作的步骤分别是______________。
5、计算题 为了测定一置于空气中的某硫酸酸化的FeSO4溶液中Fe2+被氧化的百分率,某同学准确量取pH=1(忽略Fe2+、Fe3+的水解)的FeSO4溶液200 mL,加入过量BaCl2溶液,充分反应后过滤、洗涤、干燥,得到沉淀28.0 g;再另取同样的FeSO4溶液200 mL,向其中加入过量NaOH溶液,搅拌使其充分反应,待沉淀全部变为红褐色后,过滤、洗涤并灼烧所得固体,最终得固体8.0 g。
(1)通过计算,填写下表:
c(H+)
| c(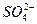 ) )
| c(Fe2+、Fe3+)
|
?
| ?
| ?
|
注:c(Fe2+、Fe3+)表示Fe2+和Fe3+的总的物质的量的浓度。
(2)计算原溶液中Fe2+被氧化的百分率。
(3)当Fe2+部分被氧化时,试推导c(Fe2+、Fe3+)与c(H+)、c(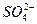 )的关系。
)的关系。