1、选择题 相同条件下,按体积比1∶1混合的气体,其平均相对分子质量为36,它们是
A.NO和NO2
B.CO和CO2
C.N2和O2
D.O2和CO
参考答案:B
本题解析:
本题难度:一般
2、选择题 为提纯下列物质(括号内为杂质),所选用的试剂和分离方法均正确的是
(?)
A.溴乙烷(乙醇):水,分液
B.氯化铵溶液(氯化铁):NaOH,过滤
C.硝酸铜溶液(硝酸银):铜粉,结晶
D.二氧化碳(二氧化硫):饱和Na2CO3,洗气
参考答案:A
本题解析:A、加水之后乙醇溶入水层(任意比),而溴乙烷不溶于水,静置分层后分液,即可分离;
B、NaOH不但和氯化铁反应,而且与氯化铵反应;
C、没有过滤……;
D、碳酸钠溶液既能与二氧化硫反应,也能与二氧化碳反应。
本题难度:一般
3、选择题 在一定条件下,萘可以被硝、硫混酸硝化生成二硝基物,它是1,5-二硝基萘(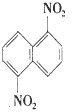 )、1,8 -二硝基萘(
)、1,8 -二硝基萘(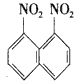 )的混合物,后者可溶于质量分数大 于98%的硫酸,而前者不能。利用这一性质可以将 这两种异构体分离,将上述硝化产物加入适量的 98%硫酸,充分搅拌,用耐酸漏斗过滤,欲从滤液中 得到同体1,8 -二硝基萘,应采用的方法是?
)的混合物,后者可溶于质量分数大 于98%的硫酸,而前者不能。利用这一性质可以将 这两种异构体分离,将上述硝化产物加入适量的 98%硫酸,充分搅拌,用耐酸漏斗过滤,欲从滤液中 得到同体1,8 -二硝基萘,应采用的方法是?
[? ]
A.蒸发浓缩结晶
B.向滤液中加水后过滤
C.用Na2CO3溶液处理滤液
D.将滤液缓缓加入水中并过滤
参考答案:D
本题解析:
本题难度:一般
4、选择题 下图为分离乙酸乙酯、乙酸和乙醇混合物的实验操作流程图

在上述实验过程中,所涉及的三次分离操作分别是
[? ]
A.①蒸馏 ②过滤 ③分液
B.①分液 ②蒸馏 ③蒸馏
C.①蒸馏 ②分液 ③分液
D.①分液 ②蒸馏 ③结晶、过滤
参考答案:B
本题解析:
本题难度:一般
5、选择题 用10mL?0.1mol?L-1?AgNO3溶液恰好可使相同体积的氯化钠、氯化铝和氯化镁三种溶液中的氯离子完全转化为氯化银沉淀,则三种盐溶液的物质的量浓度之比是
A.3:1:2
B.1:3:2
C.6:2:3
D.1:1:1
参考答案:C
本题解析:分析:用10mL?0.1mol?L-1?AgNO3溶液恰好可使相同体积的NaCl、AlCl3、MgCl2三种溶液中的氯离子完全转化为氯化银沉淀,则所生成的沉淀AgCl的物质的量相同,令AgCl的物质的量为1mol,根据氯原子守恒计算n(NaCl)、n(MgCl2)、n(AlCl3),体积相同,浓度之比等于物质的量之比.
解答:相同体积的NaCl、AlCl3、MgCl2三种溶液过量的硝酸银溶液反应,所生成的沉淀AgCl的物质的量相同,令AgCl的物质的量为1mol,根据氯原子守恒,则:
n(NaCl)=n(AgCl)=1mol
n(AlCl3)= n(AgCl)=
n(AgCl)= ×1mol=
×1mol= mol
mol
n(MgCl2)= n(AgCl)=
n(AgCl)= ×1mol=
×1mol= mol
mol
体积相同,浓度之比等于物质的量之比,故c(NaCl):c(AlCl3):c(MgCl2)=1mol: mol:
mol: mol=6:2:3,
mol=6:2:3,
故选C.
点评:本题考查物质的量浓度的有关计算,难度不大,注意利用假设法与守恒进行的计算,可以简化计算过程.
本题难度:简单