1、选择题 对水的电离平衡不产生影响的粒子是
[? ]
A.Fe3+
B.CH3COOH
C.Cl-
D.NH3・H2O
参考答案:C
本题解析:
本题难度:一般
2、填空题 (4分)水的电离平衡如图所示.
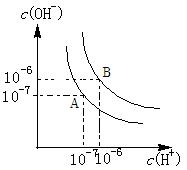
(1)若A点表示25℃时水的电离平衡状态,当升高温度至100℃时水的电离平衡状态为B点,则此时水的离子积为
(2)将100℃时p H=8的Ba(OH)2溶液与pH=5的盐酸混合,并保持100℃的恒温,欲使混合溶液的pH=7,则Ba(OH)2溶液与盐酸的体积比为
H=8的Ba(OH)2溶液与pH=5的盐酸混合,并保持100℃的恒温,欲使混合溶液的pH=7,则Ba(OH)2溶液与盐酸的体积比为 
参考答案: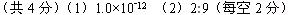
本题解析:略
本题难度:一般
3、选择题 对H2O的电离平衡不产生影响的粒子是
[? ]
A.
B.
C.
D.
参考答案:C
本题解析:
本题难度:一般
4、实验题 (12分)某学生用0.1000mol/LKOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如
下几步:
A 移取20.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
B 用标准溶液润洗滴定管2-3次
C 把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液
D.取标准KOH溶液注入碱式滴定管至0刻度以上2-3cm
E.调节液面至0或0刻度以下,记下读数
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面刻度
(1) 正确操作的顺序是(用序号字母填写) B- 。
(2) 滴定开始后,眼睛注视 ,判断滴定终点的现象是:
(3) 下列操作中可能使所测盐酸的浓度数值偏高的是
A 碱式滴定管未用标准溶液润洗就直接注入标准液
B 滴定前盛放HCl的锥形瓶用蒸馏水洗净后有少量水残留
C 碱式滴定管在滴定前有气泡,滴定后气泡消失
D 读取氢氧化钠溶液时,开始仰视读数,滴定结束时俯视读数
(4)滴定开始和结束时,碱式滴定管中的液面如图C所示,则终点读数为 mL,所测盐酸溶液的浓度为 mol/L。
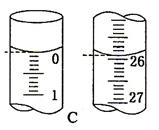
参考答案:26. (12分) (1) DCEAF (2分) (2) 锥形瓶内溶液颜色的变化(2分)
溶液由无色变为(浅)红色,且半分钟内溶液颜色不发生改变(2分,每点1分)
(3) AC(2分,选1个正确给1分,有错不给分) (4)25.90(2分) 0.1295 mol/L(2分)
本题解析:
试题分析:(1)中和滴定按照检漏、洗涤、润洗、装液、取待测液并加指示剂、滴定等顺序操作,所以正确的顺序为BDCEAF;(2) 滴定开始后,两眼应该注视锥形瓶内溶液的颜色变化;滴定时,锥形瓶中溶液的颜色由无色变浅红且保持30秒内不褪色,可说明达到滴定终点:(3)碱式滴定管未用标准溶液润洗就直接注入标准液,会导致标准液稀释,根据c(待测)=C(标)xV(标)/V(待)分析,可得c(待测)偏高,A偏高;滴定前盛放HCl的锥形瓶用蒸馏水洗净后有少量水残留,没有影响HCl的物质的量,B无影响;碱式滴定管在滴定前有气泡,滴定后气泡消失,会导致末读数据增大,结果偏高,C偏高;读取氢氧化钠溶液时,开始仰视读数,滴定结束时俯视读数,开始读数偏大,结束读数偏小,结果偏小,D错误,下列操作中可能使所测盐酸的浓度数值偏高的是A、C(4)滴定管的0刻度在上,1cm之间有10个间隔,所以终点读数为25.90mL,根据c(待测)=C(标)xV(标)/V(待)计算可得所测盐酸溶液的浓度为0.1295 mol/L。
考点:考查中和滴定等知识。
本题难度:一般
5、选择题 水的电离平衡曲线如下图所示,下列说法不正确的是

[? ]
A.图中四点Kw间的关系:A=D<C<B
B.若从A点到C点,可采用:温度不变在水中加入少量NaAc 固体
C.若从A点到D点,可采用:温度不变在水中加入少量酸
D.若处在B点所在的温度,将pH = 2的硫酸与pH=10的NaOH的两种溶液等体积混合后,溶液显中性
参考答案:B
本题解析:
本题难度:一般