1、填空题 (8分)将肥皂液分装在两支试管中,向第一支试管中加入稀硫酸,有____________产生,向第二支试管中加入MgCl2溶液,则产生____________,有关反应的离子方程式为:_____________________________________,_____________________________________。
参考答案:白色沉淀 白色沉淀
C17H35COO-+H+====C17H35COOH↓?2C17H35COO-+Mg2+====Mg(C17H35COO)2↓
本题解析:肥皂的主要成分是高级脂肪酸钠,加入稀硫酸,生成不溶于水的高级脂肪酸沉淀,加入氯化镁溶液,产生不溶于水的高级脂肪酸镁沉淀。?
本题难度:简单
2、选择题 “绿色化学”要从根本上消灭污染,是一门能彻底阻止污染产生的科学.因此设计化学反应流程时要考虑“原子经济”(即原子利用率),下列反应类型从理论上看原子利用率可达到100%的是(原子利用率是指反应物中的所有原子进入期望产物中的百分比)( )
A.分解反应
B.复分解反应
C.化合反应
D.置换反应
参考答案:C
本题解析:
本题难度:一般
3、填空题 (14分)一种“人工固氮”的新方法是在光照条件下,N2在催化剂表面与水蒸气发生反应生成NH3和氧气。已知:
化学键
| N≡N
| H―O
| N―H
| O=O
|
键能/kJ・mol-1
| 945
| 463
| 391
| 498
|
(1)请根据以上信息,写出“人工固氮”新方法的热化学方程式:_____▲______;
(2)进一步研究NH3生成量与温度的关系,部分实验数据见下表(反应时间3 h):
T/℃
| 30
| 40
| 50
|
生成NH3量/(10-6mo1/L)
| 4.8
| 5.9
| 6.0
|
①50℃时从开始到3 h内以O2物质的量浓度变化表示的平均反应速率为? ▲?;
②与目前广泛应用的工业合成氨方法相比,该方法中固氮反应速率慢。请提出可提高其反应速率且增大NH3生成量的建议(请写出两条)? ▲?、? ▲?;
(3)氨是氮肥工业的重要原料。某化肥厂生产铵态氮肥(NH4)2SO4的工业流程如下:
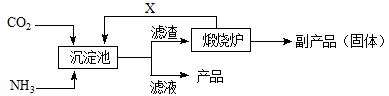
①往沉淀池中装入CaSO4悬浊液后,需先通入足量NH3,再通入CO2的原因是
? ▲?。
②煅烧炉中产生的固态副产品为? ▲?,生产流程中能被循环利用的物质X为? ▲?。
参考答案:(14分)
(1)N2(g) + 3H2O( g) 2NH3(g) +
2NH3(g) + 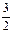 O2(g);△H =" +" 630 kJ・mol-1?(3分)
O2(g);△H =" +" 630 kJ・mol-1?(3分)
(2)①2.5×l0-8 mol/(L・min)或①1.5×l0-6 mol/(L・h)?(2分)
②升高温度;增大压强;?(合理均可,2分)
(3)①氨在水中溶解度大,使溶液呈碱性,有利于吸收CO2,增大c(CO32-),促使CaSO4转化为CaCO3,同时生成(NH4)2SO4?(3分)
②CaO(或生石灰)? CO2(或二氧化碳)?(各2分,共4分)
本题解析:略
本题难度:一般
4、选择题 下列关于工业生产的说法中,正确的是
A.工业上用氧气在接触室中氧化黄铁矿得到二氧化硫
B.工业上通过电解饱和氯化钠溶液制备金属钠
C.工业用氨氧化法制硝酸是人工固氮过程
D.生产普通玻璃的主要原料有石灰石、石英和纯碱
参考答案:D
本题解析:A.在硫酸工业中,于沸腾炉中将黄铁矿高温氧化得到二氧化硫
B.工业制钠是通过电解熔融的氯化钠得到
C.一般是通过合成氨工业来人工固氨
D.正确
本题难度:一般
5、选择题 “绿色化学”是21世纪化学发展的主导方向。“绿色化学”要求从根本上消除污染,是一门能彻底防止污染产生的科学,包括“绿色生成”和“绿色销毁”等内容。在整顿音像市场的活动中,查封了一批盗版光盘,并进行了“绿色销毁”。以下属于“绿色销毁”的是?
[? ]
A.泼上汽油焚烧
B.倾倒于江河之中
C.深埋于土中
D.碾压粉碎后回收利用
参考答案:D
本题解析:
本题难度:简单