1、选择题 将H2和N2按体积比为3∶1充入一盛有催化剂的密闭容器中,在一定条件下反应达到平衡状态,下列说法正确的是(?)
A.平衡混合气中,H2和N2的体积比一定是3∶1
B.平衡混合气中,H2和NH3的体积比一定是1∶1
C.平衡混合气中,N2和NH3的体积比一定是1∶2
D.平衡混合气中,H2、N2、NH3的体积比一定是3∶1∶2
2、选择题 已知在一密闭容器中充入1 mol CO2和3 mol H2,在高温时气体混合物达到平衡:CO2 + H2 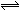 CO + H2O,已知达平衡时生成0.75 mol CO,则当H2 改为9 mol 时,在上述条件下重新达平衡时,生成CO和水蒸气物质的量之和可能为(?)
CO + H2O,已知达平衡时生成0.75 mol CO,则当H2 改为9 mol 时,在上述条件下重新达平衡时,生成CO和水蒸气物质的量之和可能为(?)
A.2.0mol
B.1.5mol
C.1.8mol
D.2.5mol
3、选择题 已知450℃时,反应H2(g)+I2(g) 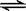 ?2HI(g)的K=50,由此推测在450℃时,反应2HI(g)
?2HI(g)的K=50,由此推测在450℃时,反应2HI(g) 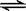 ?H2(g)+I2(g)的化学平衡常数为
?H2(g)+I2(g)的化学平衡常数为
A.50
B.0.02
C.100
D.无法确定
4、填空题 (17分)已知化学反应①:Fe(s)+CO2(g) FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)
FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)  FeO(s)+H2(g),其平衡常数为K2,在温度973 K和1 173 K情况下,K1、K2的值分别如下:
FeO(s)+H2(g),其平衡常数为K2,在温度973 K和1 173 K情况下,K1、K2的值分别如下:
温度
| K1
| K2
|
973 K
| 1.47
| 2.38
|
1173 K
| 2.15
| 1.67
|
(1)通过表格中的数值可以 推断:反应①是?(填“吸热”或“放热”)反应。
推断:反应①是?(填“吸热”或“放热”)反应。
(2)现有反应③:CO2(g)+H2(g)  CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=?,根据反应①与②可推导出K1、K2与K3之间的关系式?,据此关系式及上表数据,也能推断出反应③
CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=?,根据反应①与②可推导出K1、K2与K3之间的关系式?,据此关系式及上表数据,也能推断出反应③ 是?(填“吸热”或“放热”)反应。
是?(填“吸热”或“放热”)反应。
(3)要使反应③在一定条件下建立的平衡向正反应方向移动同时υ正增大可采取的措施
有?(填写字母序号)。
A.缩小反应容器的容积? B.扩大反应容器的容积
C.升高温度? D.使用合适的催化剂? E.设法减小平衡体系中的CO的浓度
(4)图甲、乙分别表示反应③在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:
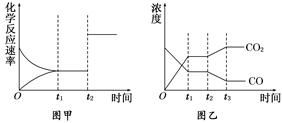
①图甲中t2时刻发生改变的条件是?。②图乙中t2时刻发生改变的条件是?。
(5)在830℃温度下,反应③的K值为1,在2 L的密闭容器中,加入1 mol CO2和3 mol H2充分反应达平衡时,CO平衡浓度为??mol/L。H2转化率?。若向容器中再加入1 mol CO2和3 mol H2 达到平衡后CO平衡浓度?mol/L ,CO2体积分数?
5、计算题 将4mol SO2和2mol O2气体在2L的密闭容器中混合,在一定条件下发生如下反应:
2SO2(g)+O2 (g)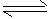 2SO3 (g)。若经过2s后测得SO3的浓度为0.6 mol/ L,
2SO3 (g)。若经过2s后测得SO3的浓度为0.6 mol/ L,
试计算:(1)用氧气表示该反应2s内的平均速率; (2)2s末SO2的转化率; (3)2s末O2浓度。