1��ѡ���� ���и���Ԫ�أ���ԭ�Ӱ뾶���μ�С��Ԫ�ص�һ�����������ߵ�˳�����е��ǣ�?��
A��K��Na��Li
B��N��O��C
C��Cl��S��P
D��Al��Mg��Na
2��ѡ���� ���ֶ�����Ԫ�ص���Ҫ���ϼۼ�ԭ�ӵ�ԭ�Ӱ뾶���ݼ��±���
Ԫ�ش���
| L
| M
| N
| R
| Q
| T
|
��Ҫ���ϼ�
| +2
| +3
| +6����2
| +7����1
| +5��+3����3
| ��2
|
ԭ�Ӱ뾶/nm
| 0��160
| 0��143
| 0��102
| 0��099
| 0��110
| 0��074
|
?�ݱ�����Ϣ�жϣ������й������У���ȷ����
A��L��M�ĵ��ʷֱ���ͬŨ�ȵ�ϡ���ᷴӦʱ��M�ĵ��ʷ�Ӧ�����ҡ�
B��M��T�γɵĻ����ﲻ������ǿ��
C����Q��R��Ԫ���γɵĻ���������и�ԭ����������������Ϊ8
D��N��T��Ԫ�ؿ����γ����ֻ�����ڱ�״���¾�Ϊ��̬
3��ѡ���� ijԪ�ص�ԭ�Ӻ�����3�����Ӳ㣬�������7�����ӣ�����ڵ�������Ϊ
A��14
B��15
C��16
D��17
4������� ��֪��A��B��C��D��E��F��XΪ���ڱ���ǰ�����ڵ�����Ԫ�أ����ǵ�ԭ��������������A�����ڱ���ԭ�Ӱ뾶��С��Ԫ�أ�B�Ļ�̬ԭ����3����ͬ���ܼ������ܼ��е�������ȣ�D�Ļ�̬ԭ��2p�ܼ��ϵ�δ�ɶԵ�������Bԭ�ӵ���ͬ��D2-������E2+���Ӿ�����ͬ���ȶ����Ӳ�ṹ��F�С����������֮�ƣ�F4+���Ӻ��ԭ�ӵĺ�������Ų���ͬ��X�Ļ�̬ԭ�ӵļ۵����Ų�ʽΪ3d84s2.
��ش��������⣺
��1��B��C��D����Ԫ�صĵ縺���ɴ�С��˳����?����Ԫ�ط��ţ���
��2����AԪ������������Ԫ���γɵķ����У�������ԭ��Ϊsp3�ӻ��ķ���ʽΪ?����д��2�ּ���
��3����Cͬ�塢��λ�ڵ�������Ԫ�����γ���̬����ĵ���ʽΪ?��������?������ԡ��Ǽ��ԡ������ӣ���е����C���⻯��ķе㣬��Ҫԭ����?��
��4��F�Ļ�̬ԭ�Ӻ�������Ų�ʽ��?��
��5��Eԭ�ӵĵ�һ�����ܱ�ͬ���ں�������Ԫ�صĵ�һ������?�����С������
��6������������������Դ��XԪ�����磨La��Ԫ�صĺϽ����������ϣ��úϽ�ľ�������ͼ��ʾ������������һ��Xԭ�ӣ�����Xԭ�Ӷ��ھ������ϣ���þ���Ļ�ѧʽΪ?����֪�þ�����ܶ�Ϊ ����Ħ������Ϊ
����Ħ������Ϊ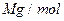 ����þ����������?�������г���ʽ��
����þ����������?�������г���ʽ��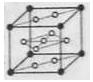
5��ѡ���� ������RO3n -�й���x ��������ӣ�R ԭ�ӵ�������ΪA ����R ԭ�Ӻ��ں��е�������Ϊ��?��
A�� A + n + 48 �C x
B��A + n + 24 �C x
C��A - n + 24 �C x
D��A - n - 24 �C x