1��ѡ���� ��������CO2����ͨ��KOH��Ba(OH)2��KAlO2�Ļ����Һ�У����ɳ�����ͨ��CO2�����Ĺ�ϵ�ɱ�ʾΪ
[? ]
A��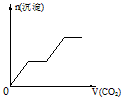
B��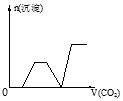
C��
D��
�ο��𰸣�C
���������
�����Ѷȣ�һ��
2��ѡ���� ������������ʵ���Ũ�ȵ����ᡢ����������Һ�ֱ���ڼס������ձ��У���������������������������������Ϊ5 ��6����ס������ձ��еķ�Ӧ������ֱܷ�Ϊ(����)
A���ס����ж���������
B��������������������
C�����������������������
D�������������������
�ο��𰸣�D
���������
��ȷ�𰸣�D
3H2SO4+2Al=Al2(SO4)3��3H2
��ô1molH2SO4��Ӧ2/3mol��ԭ��
2NaOH+2Al+2H2O=?2NaAlO2��H2
��ô1molNaOH��Ӧ1mol��ԭ��
��Ϊ�����ʵ��������Լ�����ʵ���Ҫ�������ܽ����Ҫ�ࡣ�����ᶼ��������϶�Ҳ�������෴��ֻҪ��㣬������㡣�����ü�ֵ����������
������������ô��϶�����������ֻ��Ҫ����1mol�����ܽ�1mol��������ô��������������1:1����Ϊ��ԭ������ȫ��Ӧ��Ӧ��������һ����1:1
�����㣬��ô��϶����㣬��ô������H2��������1mol��������Ӧ1mol����Ӧ1.5molH2����1mol������Ӷ�Ӧ1mol����H2.���Բ��������ı�������2:3��
ʵ�ʱ���5:6����������֮�䣬��ô�϶��Ǽ��������㡣D��ȷ��
�����Ѷȣ�һ��
3��ѡ���� 100mL 1mol��L��1���Ȼ�����Һ�м���һ�������2mol��L��1��NaOH��Һ�����ղ���3.9g������������NaOH��Һ���������Ϊ(? )
��45mL?��75mL?��100mL?��175mL
A��ֻ�Т�
B���٢�
C���ڢ�
D���ڢ�
�ο��𰸣�C
�����������AlCl3�����ʵ���Ϊ0.1mol����ȫ����Al(OH)3����ʱ����������ӦΪ7.8g���ֳ�������Ϊ3.9g��˵�������������һΪ��������ȫ��ֻ����Al(OH)3��������һ�����Ϊ���������ܽ⣬������Al(OH)3������������NaAlO2��n��Al(OH)3��=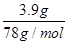 =0.05mol��
=0.05mol��
������㣬��Al3��+3OH���TAl(OH)3����֪��
NaOH�����ʵ���Ϊ0.05mol��3=0.15mol��
����NaOH��Һ�����Ϊ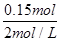 =0.075L����75mL��
=0.075L����75mL��
�ڳ��������ܽ⣬������Al(OH)3������������NaAlO2��
����? Al3��+3OH���TAl(OH)3��
0.1mol 0.3mol? 0.1mol
Al(OH)3 +OH���TAlO2��+2H2O
��0.1-0.05��mol ��0.1-0.05��mol
�����ĵļ�����ʵ���Ϊ0.3mol����0.1-0.05��mol=0.35mol������NaOH��Һ�����Ϊ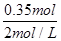 =0.175L����175mL��ѡC��
=0.175L����175mL��ѡC��
�����Ѷȣ�һ��
4������� ��ʾ��ijЩ����������������ռӦ�������Ρ��������»�ѧ��Ӧ��ͼ��գ�
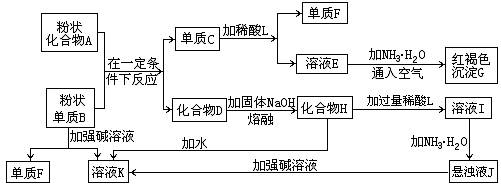
��1������F��_____________________��
��2����E����G�����ӷ�Ӧ����ʽ����ѧ����ʽ��________________________��
��3����ҺI����������������_____________________��
��4����Cת��ΪE��F������Ũ�ᣬ����ѡ�õ�Ũ���ǣ�д����ʽ��______________��
�ο��𰸣���1����1�֣�H2?
��2����2�֣�4Fe2++8NH3��H2O+O2+2H2O=4Fe(OH)3��+8NH4+
��Fe2++2NH3��H2O=Fe(OH)2��+2NH4+? 4Fe(OH)2+O2+2H2O=4Fe(OH)3
(3)��2�֣�Al3+��Na+
��(4)��1�֣�H2SO4(��HNO3)
�����������
�����Ѷȣ���
5��ѡ���� ��ʹ������Һ�е�Al3+��ȫ�������������˵��Լ��ǣ�
A��NaOH��Һ
B������
C����ˮ
D���Ȼ�����Һ
�ο��𰸣�C
��������������������ΪB��Al(OH)3����������������������ǿ����Һ����NaOH��Һ��Al3+��Ӧʱ��NaOH�����������������ȫ����������C��
ѧ��ָ����ѧϰ��������Ҫ����������ʣ��ص���ա����ۡ����ԡ�����Ĥ���� Al2O3��Al(OH)3�����ԣ������Dz�����������Һ���簱ˮ�����Ʊ�Al(OH)3ʱ������������Һ�Ͱ�ˮ��Ӧ��
�����Ѷȣ���