1��ѡ���� ����ʵ������ܴﵽĿ�Ļ��ʵ������Ӱ�����
[? ]
A����5.00?mL?12?mol/L������ϡ����500?mL�����Ƴ�0.1200?mol/L������
B������к͵ζ�ǰ���ζ����ô�װҺ����ϴ����ƿû���ô�װҺ����ϴ
C����Ũ��ˮ�м���ʯ�ң�������������ͨ��ʢ�������Ƶĸ���ܺ�õ����﴿���İ���
D����FeCl3Ũ��Һ�еμ�NaOH��Һ�����������ڣ��Ʊ�Fe(OH)3����
2������� ij�л����������г��ȼ�գ����ɵ�ˮ������CO2�����ʵ�����Ϊ1��1���ɴ˿ɵó��Ľ����ǣ�������
A��������̼����ԭ�Ӹ�����Ϊ2��1
B�����л��������C��H��O������Ϊ1��2��3
C���л����бض�����
D�����ж��л������Ƿ�����Ԫ��
3������� ijͬѧ��һ����������Cl2ǡ����ȫ��Ӧ�õ�һ��������R��Ȼ��ͨ��ʵ��ȷ����ɷ֣�̽���������£�
��1��������裺��������м��貹��������
����A���ù���������FeCl3������B��______������C��______��
��2�����ʵ�鷽����
ȡ������������R���ձ��У�������ˮ�ܽ⣬Ȼ��ȡ����R��Һ�ֱ����ʵ�飬ʵ��������������±������ڱ�������дʵ������
| ʵ�鷽�� | ʵ������ | ����
����R��Һ�м�KSCN��Һ
______
������������FeCl3
����R��Һ�еμ�����KMnO4��Һ
______
�����������FeCl2
|
�ɴ˵ó����ۣ�����______����������ĸ����
��3��д����R��Һ�еμ�����KSCN��Һ�����ӷ���ʽ��______��25��ʱ����ø÷�Ӧ��ƽ��ʱ��ƽ�ⳣ��ΪK1�������¶Ȳ��䣬�����μ�����KSCN��Һ������ƽ��ʱ�����ƽ�ⳣ��ΪK2����K1______K2�����������������=��������Һ����ɫ______������������dz�����䡱����
��4��R��Һ����ӡˢ��·ͭ��ĸ�ʴ����д���÷�Ӧ�����ӷ���ʽ��______��
4������� ��������ͼ�е�ʵ��װ�òⶨ����ͭ������һ��Ũ�ȵ�Ũ���ᷴӦ���ɵ�NO�����NO2��������ʵ���֮�ȣ���m��ʾ��������װ��C�ɹ��ƿ����������ɣ��������ɼס���������������ɣ�����Ƥ����ͨ����װ������ˮ�����п̶ȣ�0mL��50mL�����ҹܿ������ƶ����ش��������⣺
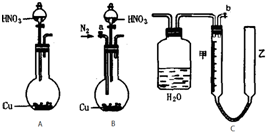
��1��ʵ�������壨NO��NO2������װ��Ӧѡ��______����װ����ţ���
��2��ʵ���е����壨NO��NO2��ͨ��Cװ�ã�������ͼ�Ĺ��ƿ�н������ܻ�����

��3��Ҫ�ⶨmֵ����Ҫ��C�е���Һ�����к͵ζ�������Ũ�������ǿ�����ԣ��ܰ����ָʾ��������ɫ��Ӱ��ʵ�飮��ˣ��к͵ζ�ǰ������еIJ�����______��
��4�����Ӻ�װ�ã���������Ժ�Ӧ����������Ҫ�IJ�������һ����b����Cװ�õ��ҹ��м�����ˮ���ڶ���______��
��5��ʵ��ǰ�ס�������Һ����ͬһˮƽ���ϣ�������ʱ�ҹܵ�Һ����ڼܵ�Һ�森��ʱӦ���еIJ�����______��
��6��ʵ���������������������������ɱ�״���£�ΪV��L����C����������ʵ���Ϊ?n?mol�����ú�n��V��ʽ�ӱ�ʾm=______������ɲ��ػ���
5��ʵ���� Ϊ�˲ⶨʯ��ʯ�Ĵ��ȣ�������ʵ��װ�ÿɹ�ѡ����֪ʯ��ʯ���������ʲ������ᷴӦ����װ��A�е�������������������Ȼ��������ˮ�������Իش������й����⣺
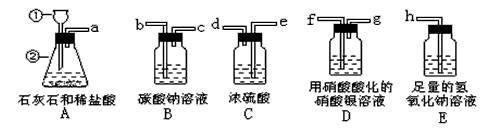
?(1)д��װ��A�������б�ŵ��������ƣ�����________��________
(2)д��װ��A�з����Ļ�ѧ��Ӧʽ________________
(3)ʵ��ʱ�й�װ�õ��ܿڵ�����˳��Ϊa��_____���x�x�x�x�Өx�x�x�x���x�x�x�x�Өx�x�x�x