1、简答题 有一白色固体粉末可能是碳酸钠、亚硫酸钠、硫酸钠中的一种或二种,某兴趣小组拟对该样品进行探究.
(1)取少量样品溶解于水,测定溶液的pH,若测得溶液的pH=7,则样品中一定含有______,一定不含______;
(2)如果要检验该样品是否含有硫酸钠,请简要说明检验的方法、现象和结论:______;
(3)取适量固体样品加入过量盐酸中,有气体放出.若要检验放出气体的组成,从以下限定试剂中选择合适的试剂设计一个组合实验分析该混合气体的组成,简要写出实验方案、现象和结论.
限定试剂:品红溶液、澄清石灰水、酸性KMnO4溶液、氢氧化钠浓溶液、饱和NaHCO3溶液.
| 实验方案 | 可能的现象和相应的结论
将混合气体依次通过盛有______、______、______的洗气瓶.
参考答案:(1)碳酸钠和亚硫酸的溶液中,因为弱离子水解导致溶液显示碱性,只有硫酸钠是不水解的盐,显中性,故答案为:硫酸钠;碳酸钠、亚硫酸钠;
(2)要检验该样品是否含有硫酸钠,只需检验其中的硫酸根离子即可,根据硫酸根离子的特征离子反应:能和钡离子反应生成不溶于盐酸的白色沉淀来进行,注意不能用硝酸,硝酸具有氧化性,能将亚硫酸根离子氧化,
故答案为:取适量固体样品加入过量盐酸中,然后加入BaCl2溶液,若有沉淀出现说明样品中有Na2SO4,若无沉淀,则说明说明样品中没有Na2SO4;
(3)取适量固体样品加入过量盐酸中,有气体放出,该气体是二氧化碳和二氧化硫中的至少一种,二氧化硫和二氧化碳均能使澄清石灰水变浑浊,在检验二氧化碳之前先检验二氧化硫的存在并将二氧化硫除净,最后用澄清石灰水来检验二氧化碳,二氧化硫的检验使用品红,除去二氧化硫可以用高锰酸钾,二氧化碳的检验用澄清石灰水,故答案为:实验方案可能的现象和相应的结论品红溶液、
(足量)酸性KMnO4溶液、(足量)澄清石灰水若品红褪色,(酸性KMnO4溶液不完全褪色,)澄清石灰水变浑浊,该气体是SO2、CO2的混合气体若品红褪色,(酸性KMnO4溶液不完全褪色,)澄清石灰水不变浑浊,该气体是SO2若品红不褪色,(酸性KMnO4溶液不褪色,)澄清石灰水变浑浊,该气体是CO2
本题解析:
本题难度:一般
2、简答题 某白色粉末可能含有K2SO4、NH4Cl、NaCl.请设计合理实验探究该白色粉末的组成.
限选实验仪器与试剂:烧杯、试管、玻璃棒、量筒、胶头滴管、药匙、酒精灯、火柴、试管夹、镊子;红色石蕊试纸、1mol?L-1硫酸、1mol?L-1硝酸、1mol?L-1盐酸、2mol?L-1NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、AgNO3溶液、蒸馏水.
完成以下实验探究过程:
(1)提出假设:
根据题意,该白色粉末的组成有______种可能的情况.
(2)设计实验方案
基于该粉末中上述三种盐均存在这一假设,设计出实验方案(不要在答题卡上作答).
(3)根据②的实验方案,叙述实验操作、预期现象和结论.
| 实验操作 | 预期现象和结论
步骤1:______
______
步骤2:______
______
步骤3:______
______
步骤4:______
______
…
______
参考答案:(1)白色粉末可以是单一成分,即是K2SO4,或者NH4Cl,或者NaCl,还可以是两种成分的混合物,即K2SO4、NH4Cl的混合物,或是NH4Cl、NaCl的混合物,还可以是三种成分K2SO4、NH4Cl、NaCl的混合物,既有7种可能的情况,
故答案为:7;
(3)氯化铵受热易分解,生成的氯化氢和氨气易化合为氯化铵固体,可以以此检验氯化铵的存在,K2SO4的检验可以用硝酸钡来检验,硫酸根离子遇到钡离子会生成白色不溶于硝酸的白色沉淀,为了防止对氯化钠检验的干扰,不用氯化钡,检验氯化钠可以采用硝酸酸化的硝酸银来检验,故答案为:
实验操作预期现象和结论步骤1:用药匙取少量白色粉末于试管A底部,点燃酒精灯,充分加热试管.白色粉末减少,有白烟生成,试管上部有白色固体凝结,说明原白色粉末含有NH4Cl.步骤2:用药匙取少量试管A中的残留固体于试管B中,滴加适量蒸馏水,振荡.固体溶解得无色溶液.步骤3:向试管B中滴加过量的?Ba(NO3)2溶液和1mol?L-1硝酸,充分振荡后静置.有白色沉淀生成,证明原白色粉末含有?K2SO4.步骤4:取试管B中上层清液少量于试管C中,滴加?AgNO3溶液和1mol?L-1硝酸.有白色沉淀生成,证明原白色粉末含有NaCl..
本题解析:
本题难度:一般
3、选择题 下列实验操作能达到目的或对实验结果的推理正确的是
[? ]
A.酸碱中和滴定前,滴定管和锥形瓶都用待装液体润洗
B.用pH试纸测定CH3COONa溶液的pH,证明CH3COOH是弱电解质
C.向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成,则该溶液中一定含有SO42-
D.将镁和铝用导线连接再插进稀NaOH溶液中,镁条上产生气泡,说明镁比铝活泼
参考答案:B
本题解析:
本题难度:一般
4、实验题 某研究小组测定菠菜中草酸及草酸盐含量(以C2O42-计),实验步骤如下:
①将菠菜样品预处理后,热水浸泡,过滤得到含有草酸及草酸盐的溶液。
②调节溶液的酸碱性,滴加足量CaCl2溶液,产生白色沉淀;加入足量醋酸,使CaCO3溶解;过滤得到CaC2O4固体。
③用稀HCl溶解CaC2O4,并加水配制成l00mL溶液。每次准确移取25.00mL 该溶液,用0.0100 mol・L-1 KMnO4标准溶液滴定,平均消耗标准溶液V mL。 回答下列问题:
(1)步骤①中“样品预处理”的方法是___________。(A.灼烧成灰B.研磨成汁)
(2)步骤②中“调节溶液的酸碱性”至___________。(A.弱碱性B.弱酸性C.中性) 验证CaCl2溶液已“足量”的操作和现象是:____________。
(3)步骤③中用到的玻璃仪器除烧杯、锥形瓶、胶头滴管、玻璃棒外,还有__________ 。
(4)经计算,该菠菜样品中C2O42-的总物质的量为__________,若样品的质量为mg,则 菠菜中草酸及草酸盐(以C2O42-计)的质量分数为___________ 。
(已知:2MnO4-+ 5C2O42-+16H+=2Mn2+ +10CO2↑+8H2O,C2O42-的摩尔质量为88 g・mol-1)
参考答案:(1)B
(2)A(或C) ;静置,待上层溶液澄清后滴入CaCl2 溶液,不出现浑浊
(3)酸式滴定管、容量瓶
(4)V×10-4 mol?;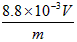 ?×100% ?×100%
本题解析:
本题难度:一般
5、实验题 现有一定量含有Na2O杂质的Na2O2试样。请从下图中选用适当的实验装置,设计一个最简单的实验,测定Na2O2试样的纯度(可供选用的反应物只有CaCO3固体,6 mol/L盐酸和蒸馏水)。

请填写下列空白:
(1)写出实验中Na2O2和Na2O分别发生反应的化学方程式:__________________。
(2)应选用的装置是A____________(只要求写出图中装置的标号)。
(3)所选用装置的连接顺序应是(填各接口的字母,连接胶管省略):____________________。
参考答案:(1)2Na2O2+2H2O===4NaOH+O2↑,Na2O+H2O===2NaOH
(2)①④⑤
(3)G-B-A-F
本题解析:
本题难度:一般
|
|