1、选择题 某同学设计如下实验测量mg铜银合金样品中铜的质量分数:
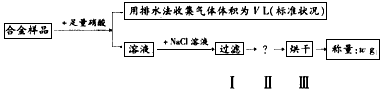
下列说法中不正确的是
[? ]
A.收集到的VL气体全为NO
B.过滤用到的玻璃仪器是:烧杯、漏斗、玻璃棒
C.操作Ⅱ应是洗涤
D.铜的质量分数为: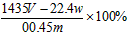
参考答案:D
本题解析:
本题难度:一般
2、实验题 粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物。进行如下实验: ?
①取适量A进行铝热反应,产物中有单质B生成; ?
②另取20g?A全部溶于0.15L?6.0mol/L盐酸中,得溶液C; ?
③将①中得到的单质B和溶液C反应,放出1.12L(标准状况)气体,同时生成的溶液D中还残留有固体物质B; ?
④用KSCN溶液检验时,溶液D不变色。 ?
请填空:?
(1)①中引发铝热反应的实验操作是____,产物中的单质B是____。?
(2)②中所发生的各反应的化学方程式是____。?
(3)③中所发生的各反应的离子方程式是____。?
(4)若溶液D的体积仍视为0.15L,则该溶液中c(Mg2+)为____,c(Fe2+)为____。
参考答案:(1)“略”?
(2)Fe2O3?+?6HCl=2FeCl3?+?3H2O、MgO?+2HCl=MgCl2?+?H2O?
(3)Fe+2H+=Fe2++H2↑、Fe+2Fe3+=3Fe2+?
(4)0.67?mol/L;2.3?mol/L
本题解析:
本题难度:一般
3、实验题 蒸馏是实验室制备蒸馏水的常用方法。
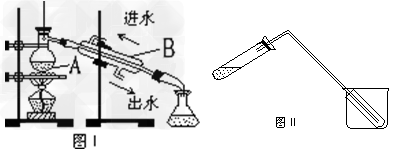
⑴图I是实验室制取蒸馏水的常用装置,图中明显的错误是______________。
⑵仪器A的名称是________,仪器B的名称是_____________。
⑶实验时A中除加入少量自来水外,还需加入少量_________,其作用是____________。图II装置也可用于少量蒸馏水的制取(加热及固定仪器略),其原理与图I完全相同。该装置中使用的玻璃导管较长,其作用是_________;烧杯中还应盛有的物质是___________。
参考答案:⑴冷凝管进出水口颠倒
⑵蒸馏烧瓶;冷凝器
⑶碎瓷片;防止液体暴沸;冷凝水蒸气;冰水
本题解析:
本题难度:一般
4、选择题 实验装置合理,能够达到实验目的是( )
A.
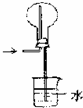
氯化氢气体的吸收
B.

模拟氯碱工业
C.
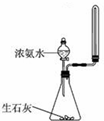
制备少量的氯气
D.
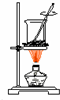
海带灼烧成灰
参考答案:A
本题解析:
本题难度:简单
5、实验题 石灰石的主要成份是碳酸钙,此外还有?SiO2?、?Fe2O3、?Al2O3等杂质。测定石灰石中钙元素的质量百分含量的流程图如下:
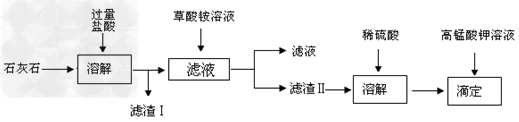
已知:草酸(H2C2O4)是一种二元弱酸。
(1)滤渣Ⅰ的成分是_________,该物质溶于氢氧化钠溶液的化学方程式为__________________________。
(2)请写出生成滤渣Ⅱ(CaC2O4・H2O)的离子方程式____________________。
(3)加入的(NH4)2C2O4?溶液要求是饱和的,其原因是____________。不仅如此,在加入饱和(NH4)2C2O4?溶液后,还需要向溶液中滴加氨水,其原因是_______________?。
(4)将草酸钙沉淀?(CaC2O4・H2O),用硫酸溶解,用a?mol/L的标准高锰酸钾溶液滴定生成的草酸,发生化学反应:H2C2O4?+?MnO4-?+?H+?→?Mn2+?+?CO2?↑+?H2O(未配平),其中还原剂是___________。若开始取用样品的质量为m?g,硫酸溶解后所得草酸溶液的体积为100mL,每次取25.00mL进行滴定,达到滴定终点时所耗KMnO4溶液体积为?b?ml(三次平均值),所得草酸溶液的物质的量的浓度是____________?;石灰石中钙元素的质量百分含量为_________。(相对原子质量:Ca-40)
参考答案:(1)SiO2;SiO2?+?2NaOH?=?Na2SiO3?+?H2O
(2)C2O42-+Ca2++H2O=CaC2O4・H2O↓
(3)保持较大的C2O42-离子浓度,使Ca2+沉淀完全;中和过量的盐酸,使溶液中?C2O42-浓度慢慢增大,可以生成CaC2O4沉淀
(4)H2C2O4;0.1ab?mol/L;0.4ab/m×100%
本题解析:
本题难度:一般